题目内容
6.现有铜和氧化铜的混合物22.4g,加入某质量分数的稀盐酸至恰好完全反应,所用稀盐酸质量100g,将反应后的固液混合物过滤,得到滤液116g,则该混合物中铜元素的质量分数为( )| A. | 28.6% | B. | 85.7% | C. | 87.5% | D. | 71.4% |
分析 由于氧化铜与盐酸反应生成氯化铜,而铜不会反应,所以滤渣即为混合物中的单质铜,据此可知混合物中的氧化铜的质量,而后可以计算出混合物中Cu元素的质量分数.
解答 解:由于氧化铜与盐酸反应生成氯化铜,而铜不会反应,所以滤渣即为混合物中的单质铜,铜的质量=100g+22.4g-116g=6.4g,氧化铜中用于氧元素的质量=(22.4g-6.4g)×$\frac{16}{80}×100%$=3.2g
则原混合物中Cu元素的质量分数=$\frac{22.4g-3.2g}{22.4g}$×100%=85.7%
故选B.
点评 此题是对化学式有关计算的考查,解题的关键是掌握有关反应的情况以及铜元素的转化,而后利用反应前后元素的质量不会改变解答即可.

练习册系列答案
相关题目
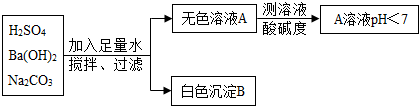
16.将下列各组物质充分混合后,所得溶液的质量比反应前溶液的质量减少的是( )
| A. | 二氧化硫与氢氧化钠溶液 | B. | 锌粉放入硫酸铜溶液中 | ||
| C. | 碳酸钠粉末和稀盐酸 | D. | 稀硫酸和氢氧化钡溶液 |
17.2015年4月16日,国务院印发《水污染防治行动计划》,该计划凸显了海域管理、水陆统筹、系统治理、协力治污和突出执法监督等“全链条”治水的特点.下列关于水资源治理的说法中不正确的是( )
| A. | 取缔不符合国家产业政策的小型农药等严重污染水环境的生产项目 | |
| B. | 限期淘汰公共建筑中不符合节水标准的生活用水器具 | |
| C. | 天然水中硬水属于混合物,软水属于纯净物 | |
| D. | 节约保护水资源,控制用水总量 |
14.对实验现象的观察和分析,有助于获得化学知识并学会科学探究的方法.下列对实验现象的分析合理的是( )
| A. | 向某无色溶液中滴入酚酞试液,溶液呈红色,则该溶液是碱溶液 | |
| B. | 向某无色溶液中滴入硝酸银溶液,产生白色沉淀,则该溶液是盐酸 | |
| C. | 把燃着的木条伸入某无色气体的集气瓶中,火焰熄灭,则该气体是二氧化碳 | |
| D. | 取某天然水于烧杯中,加入肥皂水,产生大量浮渣,则该天然水是硬水 |
1.A、B、C、D四种物质的转化关系如图所示,它们均为初中化学中常见的物质,其中A是一种黑色氧化物,B物质的溶液呈蓝色.则X可能为( )
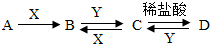
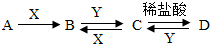
| A. | H2S04 | B. | HCl | C. | NaOH | D. | Cu(OH)2 |
11.下列说法正确的是( )
| A. | 浓溶液一定是饱和溶液 | |
| B. | 固体物质的溶解度都随温度的升高而增大 | |
| C. | 同一温度下,同一物质的饱和溶液的质量分数大于其不饱和溶液 | |
| D. | t℃时a物质的溶解度为50g,则30g该物质投入到50g水中可得80g溶液 |
2.下列变化中,属于化学变化的是( )
| A. | 石油的分馏 | B. | 浓硫酸的腐蚀 | ||
| C. | 稀有气体通电时发光 | D. | 分离液态空气制氧气 |
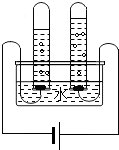 左试管中产生的是氢气,检验该气体的方法是用木条去点燃;右试管中产生的是氧气,检验该气体的方法是使用带火星的木条.由以上实验事实得出结论:说明水是由氢元素和氧元素组成的.
左试管中产生的是氢气,检验该气体的方法是用木条去点燃;右试管中产生的是氧气,检验该气体的方法是使用带火星的木条.由以上实验事实得出结论:说明水是由氢元素和氧元素组成的.