题目内容
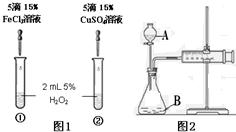
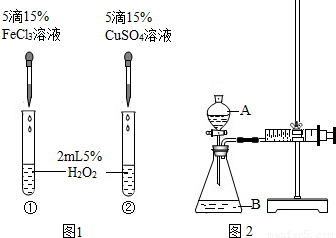
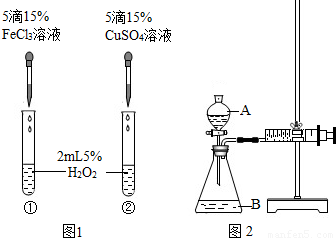
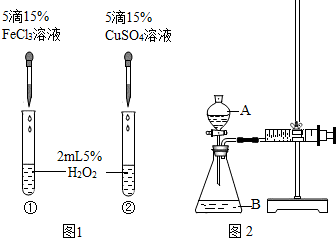
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验.下列叙述中不正确的是
- A.图1实验可通过观察产生气泡快慢来比较反应速率的大小
- B.若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
- C.用图2装置测定反应速率,可测定反应产生的气体体积及反应时间
- D.为检查图2装置的气密性,可关闭A处活塞,将注射器的活塞拉出一定距离,过一段时间后再松开活塞,观察活塞是否回到原位
B
分析:A、根据反应的剧烈程度与实验现象的关系判断.
B、根据催化剂的定义和作用及控制变量的情况判断.
C、根据反应速率的含义判断.
D、根据气密性检查的原理判断.
解答:A、反应的剧烈程度与实验现象有关,反应越剧烈,产生气体的速率越快,产生气泡越快,所以正确.
B、催化剂能改变化学反应的速率,这里是加快速率,若图1所示实验中反应速率为①>②,则一定说明氯化铁比硫酸铜催化效果好,因二者所含的阴离子不同,要证明Fe3+比Cu2+对H2O2分解催化效果好,还要使选择的试剂中阴离子种类相同,所以错误.
C、反应速率可用单位时间内产生的气体体积表示,该装置可通过注射器活塞的位置变化看生成气体的体积,所以正确.
D、检查装置的气密性一般是利用气压的原理,在图2装置中,关闭A处活塞,将注射器的活塞拉出一定距离,过一段时间后再松开活塞,如活塞回到原位,说明气密性良好,否则漏气,所以正确.
故选B.
点评:催化剂和催化作用是初中化学中较难理解的两个基本概念,理解掌握催化剂“一变,两不变”的特点是解题的关键.
分析:A、根据反应的剧烈程度与实验现象的关系判断.
B、根据催化剂的定义和作用及控制变量的情况判断.
C、根据反应速率的含义判断.
D、根据气密性检查的原理判断.
解答:A、反应的剧烈程度与实验现象有关,反应越剧烈,产生气体的速率越快,产生气泡越快,所以正确.
B、催化剂能改变化学反应的速率,这里是加快速率,若图1所示实验中反应速率为①>②,则一定说明氯化铁比硫酸铜催化效果好,因二者所含的阴离子不同,要证明Fe3+比Cu2+对H2O2分解催化效果好,还要使选择的试剂中阴离子种类相同,所以错误.
C、反应速率可用单位时间内产生的气体体积表示,该装置可通过注射器活塞的位置变化看生成气体的体积,所以正确.
D、检查装置的气密性一般是利用气压的原理,在图2装置中,关闭A处活塞,将注射器的活塞拉出一定距离,过一段时间后再松开活塞,如活塞回到原位,说明气密性良好,否则漏气,所以正确.
故选B.
点评:催化剂和催化作用是初中化学中较难理解的两个基本概念,理解掌握催化剂“一变,两不变”的特点是解题的关键.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴等浓度 FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡;试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生. |
(2)实验①的目的是______.
实验中滴加FeCl3溶液的目的是______.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是______(用实验中提供的试剂).
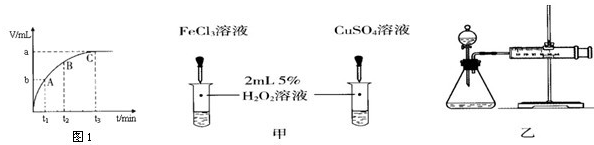
(4)某同学在50mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积与反应时间的关系如图1所示,则A、B、C三点所表示的瞬时反应速率最慢的是______.
(5)催化剂是化学反应前后______ 均未改变的一类化学物质.
(6)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:

①定性分析:如图甲可通过观察______,定性比较得出结论.有同学提出将FeCl3改为______更为合理,其理由是______.
②定量分析:用图乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是______.