题目内容
20.某化学研究小组的同学对金属铁、铝、铜进行系列研究.(1)合金的应用是人类社会文明发展的象征.有下列三种合金:①铁合金;②铝合金;③铜合金,
这三种合金被广泛应用的先后顺序按年代由远及近排列应是③①②(填序号).
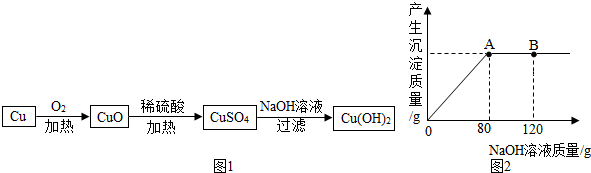
(2)该小组的同学还利用单质铜制取Cu(OH)2,其设计方案如图1:
取一定量的CuO放入盛有一定量稀硫酸的烧杯中,恰好完全反应.向烧杯中逐滴加入10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液质量的关系曲线如图2所示,当滴入10%的NaOH溶液120g时(即B点),试通过计算,求此时所得Cu(OH)2沉淀的质量(计算结果精确至0.1g).
分析 (1)人类使用金属的顺序正好和金属的活动性相反,金属活动性越强的金属越难冶炼,可以据此解答;
(2)根据化学方程式利用氢氧化钠的质量进行计算.
解答 解:(1)活动性弱的金属不易发生化学反应,能以单质形式存在,并比较容易冶炼,故人类使用金属的顺序正好和金属的活动性相反,所以,人类开始使用这三种金属的先后排序为 Cu、Fe、Al;
故答案为:③①②;
(2)设所得Cu(OH)2沉淀的质量为x
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
80 98
80g×10% x
$\frac{80}{80g×10%}$=$\frac{98}{x}$
x=9.8g
答:所得Cu(OH)2沉淀的质量为9.8g
故答案为:(1)③①②
(2)沉淀的质量为9.8g
点评 本题考查了金属的活动性顺序及其运用,熟练掌握化学方程式的计算是解题的关键.

练习册系列答案
相关题目
10.下列物质与水混合,能形成溶液的是( )
| A. | BaSO4 | B. | Cu(OH)2 | C. | NaNO3 | D. | CaCO3 |
11.下列实验设计不能达到实验目的是( )
| A. | 加入过量稀盐酸除去氢氧化钠溶液中混有的少量碳酸钠 | |
| B. | 用高温煅烧的方法除去生石灰中的石灰石 | |
| C. | 加入熟石灰,然后用研磨的方法鉴别氯化钾与氯化铵固体 | |
| D. | 用水鉴别碳酸钙和氢氧化钠两种粉末状固体 |
8.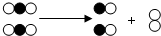 如图是表示物质间发生的一种化学反应模型示意图,图中“
如图是表示物质间发生的一种化学反应模型示意图,图中“ 、
、 ”分别表示两种不同元素的原子.该反应的类型属于( )
”分别表示两种不同元素的原子.该反应的类型属于( )
 如图是表示物质间发生的一种化学反应模型示意图,图中“
如图是表示物质间发生的一种化学反应模型示意图,图中“ 、
、 ”分别表示两种不同元素的原子.该反应的类型属于( )
”分别表示两种不同元素的原子.该反应的类型属于( )| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
15.常见金属活动性顺序如图.下列各组物质间能发生反应的是( )
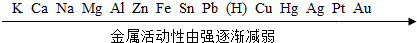
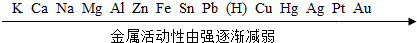
| A. | 铜和硝酸钠溶液 | B. | 铝和硫酸铜溶液 | C. | 锌和氯化钾溶液 | D. | 银和稀硫酸 |