题目内容
 某溶液中可能含有碳酸钠、氯化钾、硫酸钠、硫酸中的一种或几种,为测定其组成,进行如下实验:
某溶液中可能含有碳酸钠、氯化钾、硫酸钠、硫酸中的一种或几种,为测定其组成,进行如下实验:取样20g,先后逐滴加入氯化钡溶液、稀硝酸,产生沉淀的质量与时间的关系如图所示.
(1)实验中,AB之间图象所对应的溶液中的溶质一定有
(2)BC段沉淀减少的原因是
(3)由上述实验可知,原溶液中一定含有
(4)求原溶液中硫酸钠的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据坐标分析沉淀是先增加到A,随着氯化钡的加入,沉淀不再增加;从B点到C点沉淀又逐渐减少,说明沉淀是部分溶解于稀硝酸,因此产生的沉淀既有碳酸钡又有硫酸钡,故原溶液中肯定含有碳酸钠,同时说明没有硫酸,一定含有硫酸钠,可能含有氯化钾;据此分析解题即可.
解答:解:(1)AB之间图象说明是氯化钡和碳酸钠、硫酸钠反应后过量的情况,因此所对应的溶液中的溶质一定有过量的氯化钡和反应生成的氯化钠;
故答案为:NaCl和BaCl2;
(2)BC段减少的沉淀是能够溶于稀硝酸的碳酸钡沉淀,而硫酸钡不溶于稀硝酸,所以到C点后沉淀不在减少,化学方程式为:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O;
故答案为:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O;
(3)根据坐标分析沉淀是先增加到A,随着氯化钡的加入,沉淀不再增加;从B点到C点沉淀又逐渐减少,说明沉淀是部分溶解于稀硝酸,因此产生的沉淀既有碳酸钡又有硫酸钡,故原溶液中肯定含有碳酸钠,同时说明没有硫酸,一定含有硫酸钠,可能含有氯化钾;
故答案为:Na2CO3和Na2SO4;KCl;
(4)设原溶液中硫酸钠的质量为x
Na2SO4+BaCl2═BaSO4↓+2NaCl
142 233
x 4.66g
=
x=2.84g
原溶液中硫酸钠的质量分数:
×100%=14.2%
答:原溶液中硫酸钠的质量分数为14.2%.
故答案为:NaCl和BaCl2;
(2)BC段减少的沉淀是能够溶于稀硝酸的碳酸钡沉淀,而硫酸钡不溶于稀硝酸,所以到C点后沉淀不在减少,化学方程式为:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O;
故答案为:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O;
(3)根据坐标分析沉淀是先增加到A,随着氯化钡的加入,沉淀不再增加;从B点到C点沉淀又逐渐减少,说明沉淀是部分溶解于稀硝酸,因此产生的沉淀既有碳酸钡又有硫酸钡,故原溶液中肯定含有碳酸钠,同时说明没有硫酸,一定含有硫酸钠,可能含有氯化钾;
故答案为:Na2CO3和Na2SO4;KCl;
(4)设原溶液中硫酸钠的质量为x
Na2SO4+BaCl2═BaSO4↓+2NaCl
142 233
x 4.66g
| 142 |
| 233 |
| x |
| 4.66g |
x=2.84g
原溶液中硫酸钠的质量分数:
| 2.84g |
| 20g |
答:原溶液中硫酸钠的质量分数为14.2%.
点评:图象题是计算题中的重点也是难点,对这类题目的解决方法是能够正确分析图象所给出的信息并加以利用.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、中和反应有盐和水生成,所以有盐和水生成的化学反应一定是中和反应 |
| B、单质只含一种元素,所以含一种元素的物质一定是单质 |
| C、燃烧需要同时满足三个条件才能发生,所以灭火也一定要同时控制这三个条件 |
| D、碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性 |

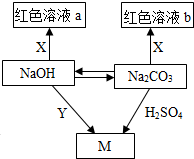 同学们在学习了碱和盐的性质后构建了如图所示的知识网络,其中“→”表示物质之间的转化关系,方框内物质含有相同的金属离子.
同学们在学习了碱和盐的性质后构建了如图所示的知识网络,其中“→”表示物质之间的转化关系,方框内物质含有相同的金属离子.