题目内容
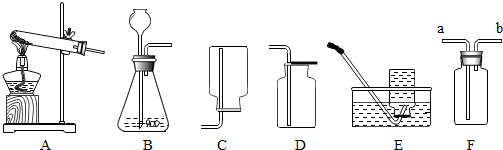
15.以下说法不正确的是( )| A. | 稀释浓硫酸时应将水缓慢倒入浓硫酸中 | |
| B. | 浓盐酸易挥发,在空气中易形成白雾 | |
| C. | 钢铁生锈时发生了化学变化 | |
| D. | 水在通常情况下是无色液体属于水的物理性质 |
分析 A、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
B、根据浓盐酸具有挥发性,进行分析判断.
C、钢铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果.
D、物理性质是不需要发生化学变化就能表现出来的性质,包括物质的颜色、状态、气味、熔点、沸点、密度、溶解性等.
解答 解:A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中,故选项说法错误.
B、浓盐酸具有挥发性,在空气中易形成白雾,故选项说法正确.
C、钢铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,生成铁锈,有新物质生成,属于化学变化,故选项说法正确.
D、水在通常情况下是无色液体,描述的是颜色、状态,不需要通过化学变化就能表现出来,属于物理性质,故选项说法正确.
故选:A.
点评 本题难度不大,掌握浓硫酸的稀释方法、浓盐酸具有挥发性、铁锈蚀的原理、物理性质等是正确解答本题的关键.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
5. 如图是元素周期表提供的铱元素的部分信息,下列说法不正确的是( )
如图是元素周期表提供的铱元素的部分信息,下列说法不正确的是( )
 如图是元素周期表提供的铱元素的部分信息,下列说法不正确的是( )
如图是元素周期表提供的铱元素的部分信息,下列说法不正确的是( )| A. | 铱原子的原子序数为77 | B. | 铱原子的质子数为77 | ||
| C. | 铱原子的中子数为77 | D. | 铱的相对原子质量为192.2 |
6.下列化学用语书写正确的是( )
| A. | 两个氢原子:H2 | B. | 3个氨分子:3NH3 | ||
| C. | 碳酸根离子:CO3-2 | D. | 氯化钙:CaCl |
20.物质的用途与性质密切相关.下列叙述错误的是( )
| A. | 因为氮气化学性质不活泼,所以可用于食品包装内防腐 | |
| B. | 因为熟石灰能和酸发生反应,所以可用熟石灰改良酸性土壤 | |
| C. | 因为“洗洁精”有乳化功能,所以可用“洗洁精”可用来洗涤餐具上的油污 | |
| D. | 因为甲醛能使蛋白质变性,可起到防腐作用,所以可用甲醛水溶液可用于浸泡水产品 |
7.金属R能发生如下反应:R+CuSO4=Cu+RSO4,下列说法错误的是( )
| A. | 该反应为置换反应 | B. | R的金属活动性比Cu强 | ||
| C. | 金属R不可能是Al | D. | 若R为Fe,则反应后溶液变为黄色 |
4.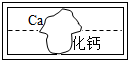 在学习酸、碱、盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
在学习酸、碱、盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
探究二:过滤后澄清滤液中会有哪些溶质?
【提出猜想】
猜想一:NaOH和Na2CO3;
猜想二:NaOH和Ca(OH)2;
猜想三:NaOH.
(3)【实验验证】同学们针对“猜想一”进行如下实验:
他们的实验结论是否正确?否(填“是”或“否”)
(4)【继续探究】设计如下实验方案确定滤液中溶质的组成.
(5)【反思与拓展】
①为防止标签被腐蚀而破损,倾倒液体时标签要向着手心.
②在分析反应后所得溶液中溶质时,除考虑可溶性的生成物,还应考虑反应的程度(合理即可).
 在学习酸、碱、盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
在学习酸、碱、盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴入酚酞试液 | 溶液变红 | 猜想①正确 |
【提出猜想】
猜想一:NaOH和Na2CO3;
猜想二:NaOH和Ca(OH)2;
猜想三:NaOH.
(3)【实验验证】同学们针对“猜想一”进行如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | “猜想一”不成立 |
(4)【继续探究】设计如下实验方案确定滤液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液,B中加入Na2CO3溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
| 若A中没有沉淀,B中产生白色沉淀 | “猜想二”成立 | |
| 若A、B中都没有沉淀产生 | “猜想三”成立 |
①为防止标签被腐蚀而破损,倾倒液体时标签要向着手心.
②在分析反应后所得溶液中溶质时,除考虑可溶性的生成物,还应考虑反应的程度(合理即可).
5.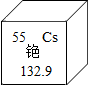 铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )
铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )
 铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )
铯原子钟300年误差不超过5秒.铯元素在周期表的信息如图,下列说法正确的是( )| A. | 铯元素属于非金属元素 | B. | 铯原子的质子数是55 | ||
| C. | 铯元素符号为CS | D. | 铯原子的相对原子质量为132.9g |