题目内容
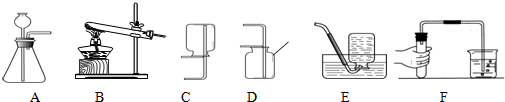
为探究燃烧的条件,小花同学查阅资料得知:白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,红磷着火点为240℃.然后她进行了如图实验:

(1)按A装置进行实验,可观察到的现象为铜片上的红磷 ,铜片上的白磷 ,水下的白磷 ;
(2)在使用组装好的B装置前首先应该进行的操作是 ,然后加入药品并将B和C装置连接,滴入双氧水,B装置中反应的化学方程式为 ,其中Mn02的作用是 ,C装置中水下的白磷
(3)从以上实验分析得出,燃烧需要的条件为:可燃物、 和 .

(1)按A装置进行实验,可观察到的现象为铜片上的红磷
(2)在使用组装好的B装置前首先应该进行的操作是
(3)从以上实验分析得出,燃烧需要的条件为:可燃物、
考点:燃烧的条件与灭火原理探究,实验室制取氧气的反应原理,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)由题意,白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,红磷着火点为240℃;根据燃烧的条件的实验现象进行分析解答即可.
(2)根据实验室制取氧气的实验步骤、反应原理、燃烧的条件进行分析解答即可.
(3)由实验(1)、(2)的实验现象,结合(2)通入氧气后水下的白磷能燃烧,进行分析解答.
(2)根据实验室制取氧气的实验步骤、反应原理、燃烧的条件进行分析解答即可.
(3)由实验(1)、(2)的实验现象,结合(2)通入氧气后水下的白磷能燃烧,进行分析解答.
解答:解:(1)由题意,白磷为蜡状固体,有剧毒,不溶于水,着火点为40℃,红磷着火点为240℃;按A装置进行实验,温度最多只有80℃,没有达到燃烧所需要的最低温度(240℃);铜片上的白磷,温度近似为80℃,已满足燃烧所需要的40℃,并且处于空气中与氧气接触充分;水中的白磷不能和氧气接触;故可观察到的现象为铜片上的红磷不燃烧,铜片上的白磷燃烧,铜片上的白磷不燃烧.
(2)在使用组装好的B装置前首先应该进行的操作是检查装置的气密性,然后再装入药品,以避免装入药品后发现装置气密性不好,更换部分仪器而浪费药品.
B装置中双氧水在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
2H2O+O2↑;其中二氧化锰起催化作用;若按B装置进行实验,水下的白磷温度达到了着火点,通入氧气后能燃烧.
(3)铜片上的白磷和红磷进行对比,可以得出燃烧需要温度达到着火点;铜片上的白磷与水中白磷比较,可以得出燃烧需要与氧气接触.
故答案为:(1)不燃烧,燃烧,不燃烧; (2)检查装置的气密性,2H2O2
2H2O+O2↑,催化作用,燃烧;(3)与氧气接触;温度达到着火点.
(2)在使用组装好的B装置前首先应该进行的操作是检查装置的气密性,然后再装入药品,以避免装入药品后发现装置气密性不好,更换部分仪器而浪费药品.
B装置中双氧水在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
| ||
(3)铜片上的白磷和红磷进行对比,可以得出燃烧需要温度达到着火点;铜片上的白磷与水中白磷比较,可以得出燃烧需要与氧气接触.
故答案为:(1)不燃烧,燃烧,不燃烧; (2)检查装置的气密性,2H2O2
| ||
点评:本题难度不大,掌握燃烧的条件(需要同时满足三个条件:①可燃物、②氧气或空气、③温度要达到着火点)是正确解答本题的关键.

练习册系列答案
相关题目
下列变化一定属于化学变化的是( )
| A、固体碘受热后变成紫红色碘蒸气 |
| B、通常状况下的氧气通过低温加压变成了淡蓝色液体 |
| C、打开浓盐酸瓶盖,从瓶口涌出白雾 |
| D、澄清石灰水露置空气中后液面产生了一层白膜 |
下列关于空气成分的说法正确的是( )
| A、氧气约占空气质量的21% |
| B、饼干在空气中变软是因为空气中含有水蒸气 |
| C、稀有气体通电发光是化学变化 |
| D、空气中的氧气主要来自植物的呼吸作用 |
 医生给病人输液时,常用葡萄糖注射液.如图为葡萄糖注射液的部分标签图,根据下图回答下列问题:
医生给病人输液时,常用葡萄糖注射液.如图为葡萄糖注射液的部分标签图,根据下图回答下列问题: