题目内容
18. 氢氧化钙溶液俗称熟石灰,在生产和生活中有广泛的用途.请根据所学化学知识回答下列问题:
氢氧化钙溶液俗称熟石灰,在生产和生活中有广泛的用途.请根据所学化学知识回答下列问题:(1)Ca(OH)2中钙元素的化合价为+2.用熟石灰配成的石灰浆可以粉刷墙壁.干燥后墙面会变硬,这时白色墙面的主要成分是D.(填选项)
A.Ca B.CaO C.Ca(OH)2 D.CaCO3
(2)用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”,“黑白粉”比熟石灰更高效,是由于其与水混合后,会恰好完全反应生成碱性更强的KOH.使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体.
①请写出“黑白粉”在水中发生的化学反应方程式Ca(OH)2+K2CO3=CaCO3↓+2KOH.
②“黑白粉”中有能够促使作物生长健壮、茎秆粗硬的重要营养素,它是K(填元素符号).
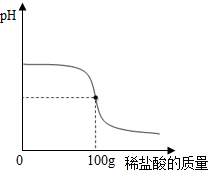
③某同学将“黑白粉”充分溶于水后,过滤,向所得滤液中滴加溶质质量分数为14.6%的稀盐酸.所加稀盐酸与溶液pH的关系如图所示.求溶液恰好为中性时,所得溶液中溶质的质量.
分析 (1)根据化合价代数和为零进行分析;
根据氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水进行分析;
(2)①根据碳酸钾和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾进行分析;
②根据植物需要的营养元素有N、P、K,“黑白粉”中含有K元素进行分析;
③根据氢氧化钾和盐酸反应生成氯化钾和水,依据题中的数据进行计算.
解答 解:(1)Ca(OH)2中氢氧根离子显示-1价,所以钙元素的化合价为+2,用熟石灰配成的石灰浆可以粉刷墙壁.干燥后墙面会变硬,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,这时白色墙面的主要成分是碳酸钙,故选:D;
(2)①碳酸钾和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾,化学方程式为:Ca(OH)2+K2CO3=CaCO3↓+2KOH;
②植物需要的营养元素有N、P、K,“黑白粉”中含有K元素;
③设所得溶液中溶质的质量为x
KOH+HCl=KCl+H2O
36.5 74.5
14.6%×100g x
$\frac{36.5}{14.6%×100g}$=$\frac{74.5}{x}$
x=29.8g
故答案为:(1)+2,D;
(2)①Ca(OH)2+K2CO3=CaCO3↓+2KOH;
②K;
③29.8g.
点评 本题主要考查化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.下列关于分子、原子的说法不正确的是( )
| A. | 它们的最主要区别是:分子可再分而原子不可再分 | |
| B. | 分子是由原子构成的 | |
| C. | 原子是化学变化中最小的粒子 | |
| D. | 分子、原子都是构成物质的基本粒子 |
3.实验室用锌粒和稀硫酸制取氢气,下列是某同学的实验操作,正确的是( )
| A. |  检查装置的气密性 | B. |  加入锌粒 | ||
| C. |  加入稀硫酸 | D. |  收集气体 |
8.宏观和微观之间建立联系是化学特有的思维方式.下列对宏观事实的微观解释中,错误的是( )
| A. | 物质的三态变化--分子的间隔发生了改变 | |
| B. | 端午时节粽飘香--分子在不断的运动 | |
| C. | 过氧化氢分解制氧气--分子在化学变化中可以再分 | |
| D. | 金刚石和石墨物理性质差异大--碳原子的结构不同 |
