题目内容
12.下列气体中.参与绿色植物光合作用的是( )| A. | SO2 | B. | CO2 | C. | N2 | D. | CH4 |
分析 根据二氧化碳是绿色植物光合作用的原料进行解答.
解答 解:A、二氧化碳是绿色植物光合作用的原料,二氧化硫容易造成酸雨,故A错误;
B、二氧化碳是绿色植物光合作用的原料,故B正确;
C、二氧化碳是绿色植物光合作用的原料,氮气的化学性质稳定,不参与绿色植物光合作用,故C错误;
D、二氧化碳是绿色植物光合作用的原料,甲烷属于可燃性气体,不参与绿色植物光合作用,故D错误.
故选:B.
点评 本题考查常见气体性质和作用,属于基础知识,只要同学们细心即可做好此题.

练习册系列答案
相关题目
2.某化学兴趣小组围绕“酸碱中和反应”,在老师引导下开展探究活动.
探究Ⅰ:证明氢氧化钠溶液与稀盐酸确实能发生反应.
【方案1】测定稀盐酸与NaOH溶液混合前后的pH.
测定某NaOH溶液的pH,pH大于7.将一定量的稀盐酸加入该NaOH溶液中,混合均匀后测定其pH,发现pH减小了,但仍然大于7,小组中有的同学认为根据这个测定结果可以认为稀盐酸与NaOH溶液发生了反应,你认为他们的结论是否正确:不正确,理由滴加的盐酸中含水,加入后使NaOH溶液变稀,同样会使溶液碱性减弱,pH减小.经过讨论后,他们向溶液中又加入一定量的稀盐酸,混合均匀后测定其pH,pH小于7.
结论:稀盐酸与氢氧化钠溶液发生了化学反应,并且稀盐酸过量.
【方案2】借助于无色酚酞试液.
【药品仪器】(如图1)
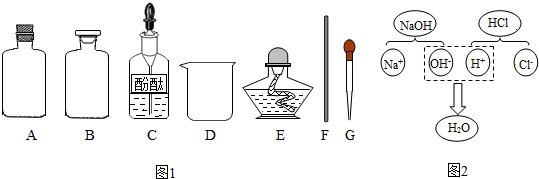
①取A(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用胶头滴管向①中溶液滴加稀盐酸,红色消失;
③用F蘸取②中溶液,在酒精灯上灼烧,有白色固体产生.
【思考拓展】
(1)如不使用酸碱指示剂,进一步确认步骤③中的白色固体不是氢氧化钠的方法是:取②中溶液,向其中滴加硫酸铜溶液,无蓝色沉淀
(2)探究步骤②中无色溶液中稀盐酸是否过量.
根据上述反应过程中溶液变成无色,不能确定稀盐酸是否过量,兴趣小组同学又分别选取了AgNO3溶液、紫色石蕊试液、铁粉设计实验方案,请你分析并判断:
方案③中反应的化学方程式Fe+2HCl=FeCl2+H2↑.上述设计方案中,不正确的是①(填“①”、
“②”或“③”),错误的原因是氯化钠溶液中也含Cl-,与硝酸银溶液反应也会生成白色沉淀.
请你再设计一个与上述实验不同原理的方案以确定稀盐酸是否过量,你选用的试剂是加入氧化铜或碳酸钠溶液.
(3)探究Ⅱ:从微观的角度认识物质及其变化的本质.图2表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是H+、OH-结合生成水.
探究Ⅰ:证明氢氧化钠溶液与稀盐酸确实能发生反应.
【方案1】测定稀盐酸与NaOH溶液混合前后的pH.
测定某NaOH溶液的pH,pH大于7.将一定量的稀盐酸加入该NaOH溶液中,混合均匀后测定其pH,发现pH减小了,但仍然大于7,小组中有的同学认为根据这个测定结果可以认为稀盐酸与NaOH溶液发生了反应,你认为他们的结论是否正确:不正确,理由滴加的盐酸中含水,加入后使NaOH溶液变稀,同样会使溶液碱性减弱,pH减小.经过讨论后,他们向溶液中又加入一定量的稀盐酸,混合均匀后测定其pH,pH小于7.
结论:稀盐酸与氢氧化钠溶液发生了化学反应,并且稀盐酸过量.
【方案2】借助于无色酚酞试液.
【药品仪器】(如图1)

①取A(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用胶头滴管向①中溶液滴加稀盐酸,红色消失;
③用F蘸取②中溶液,在酒精灯上灼烧,有白色固体产生.
【思考拓展】
(1)如不使用酸碱指示剂,进一步确认步骤③中的白色固体不是氢氧化钠的方法是:取②中溶液,向其中滴加硫酸铜溶液,无蓝色沉淀
(2)探究步骤②中无色溶液中稀盐酸是否过量.
根据上述反应过程中溶液变成无色,不能确定稀盐酸是否过量,兴趣小组同学又分别选取了AgNO3溶液、紫色石蕊试液、铁粉设计实验方案,请你分析并判断:
| 实验方案 | 实验步骤 | 现 象 | 结 论 |
| ① | 取样,加入适量的AgNO3溶液 | 出现白色沉淀 | 稀盐酸过量 |
| ② | 取样,加入几滴紫色石蕊试液 | 溶液变红 | 稀盐酸过量 |
| ③ | 取样,加入少量铁粉 | 黑色固体溶解,产生气泡,溶液变浅绿色 | 稀盐酸过量 |
“②”或“③”),错误的原因是氯化钠溶液中也含Cl-,与硝酸银溶液反应也会生成白色沉淀.
请你再设计一个与上述实验不同原理的方案以确定稀盐酸是否过量,你选用的试剂是加入氧化铜或碳酸钠溶液.
(3)探究Ⅱ:从微观的角度认识物质及其变化的本质.图2表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是H+、OH-结合生成水.
20. 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,○代表一个氢原子,
代表一个碳原子,○代表一个氢原子, 代表一个氧原子,下列说法不正确的是( )
代表一个氧原子,下列说法不正确的是( )
 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 代表一个碳原子,○代表一个氢原子,
代表一个碳原子,○代表一个氢原子, 代表一个氧原子,下列说法不正确的是( )
代表一个氧原子,下列说法不正确的是( )| A. | 乙酸是一种化合物 | |
| B. | 乙酸的相对分子质量为60 | |
| C. | 乙酸中碳元素的质量分数为60% | |
| D. | 乙酸分子中的碳原子、氢原子、氧原子的个数比为1:2:1 |
17.下列反应的化学方程式正确的是( )
| A. | 石灰水长期存放后产生的白膜用硝酸清洗:Ca(OH)+HNO3═CaNO3+2H2O | |
| B. | 硫酸铵与烧碱混合:NH4SO4+NaOH═NaSO4+H2O+NH3↑ | |
| C. | 制取铝:3Zn+Al2(SO4)3═3ZnSO4+2Al | |
| D. | 铜表面的铜绿[Cu2(OH)2CO3]用盐酸除去:Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑ |
4.已知:氯化钠和硝酸钾在不同温度下的溶解度如下表.
(1)氯化钠和硝酸钾的溶解度随温度变化趋势更大的是硝酸钾;T℃时,二者饱和溶液的溶质质量分数相等,则T介于20℃~30℃之间(从上表温度中选取最近的两个数值).
(2)80℃时,将氯化钠和硝酸钾各100g的混合物,加入到100g水中,充分搅拌,不能完全溶解的物质是氯化钠;将所得溶液冷却到10℃时,溶液的质量是156.7g.
| 温度 溶解度/g 物质 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
(2)80℃时,将氯化钠和硝酸钾各100g的混合物,加入到100g水中,充分搅拌,不能完全溶解的物质是氯化钠;将所得溶液冷却到10℃时,溶液的质量是156.7g.
1.下列四个实验中只需要完成三个就可以证明Zn、Cu、Ag三种金属的活动性顺序,其中不必进行的实验是( )
| A. | 将锌片放入稀硫酸 | B. | 将铜片放入稀硫酸 | ||
| C. | 将铜片放入硝酸银溶液 | D. | 将锌片放入硝酸银溶液 |
2.正确的实验操作对实验结果、人身安全都非常重要.下列实验操作正确合理的是( )
| A. |  量取9.5mL液体 | B. |  测定溶液的pH | ||
| C. |  闻气体气味 | D. |  点燃酒精灯 |

