题目内容
13.下列A~E五种物质由氢、碳、氧、钠、钙5种元素中的2种或3种组成.(1)A在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产,A的俗称是纯碱(或苏打).
(2)B、C两种物质的组成元素相同,且B能发生分解反应生成C,B的化学式为H2O2.
(3)D是常用的干燥剂,将D加入到E的饱和溶液中,溶液变浑浊,发生反应的化学方程式是CaO+H2O=Ca(OH)2.
(4)将A、E两种溶液混合,反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.充分反应后过滤,向滤液中加入足量稀盐酸,出现气泡,该滤液中的溶质有Na2CO3、NaOH.
分析 (1)根据碳酸钠广泛应用于玻璃、造纸、纺织和洗涤剂的生产回答;
(2)根据B、C两种物质的组成元素相同,且B能发生分解反应生成C,结合过氧化氢分解产生水和氧气回答;
(3)D是常用的干燥剂,将D加入到E的饱和溶液中,溶液变浑浊,因此D是氧化钙;
(4)根据碳酸钠和氢氧化钙的反应写出反应的方程式;根据充分反应后过滤,向滤液中加入足量稀盐酸,出现气泡,因此说明碳酸钠过量.
解答 解:(1)碳酸钠广泛应用于玻璃、造纸、纺织和洗涤剂的生产,俗名纯碱(或苏打);故填:纯碱(或苏打);
(2)B、C两种物质的组成元素相同,且B能发生分解反应生成C,过氧化氢分解产生水和氧气,因此是过氧化氢;故填:H2O2
(3)D是常用的干燥剂,将D加入到E的饱和溶液中,溶液变浑浊,因此D是氧化钙,氧化钙和水反应产生氢氧化钙,氢氧化钙不能溶解,因而出现浑浊的现象;故填:CaO+H2O=Ca(OH)2
(4)碳酸钠和氢氧化钙反应产生碳酸钙沉淀和氢氧化钠,反应的方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;充分反应后过滤,向滤液中加入足量稀盐酸,出现气泡,因此说明碳酸钠过量,因此滤液中含有生成的氢氧化钠和过量的碳酸钠;
故答案为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;Na2CO3、NaOH.
点评 本题的推断由组成物质的元素做为限定条件,因此,熟悉常见物质的组成、性质及变化规律对该题中所涉及物质的推断就至关重要了.

练习册系列答案
相关题目
3.下列图象能正确反映对应变化关系的是( )
| A. | 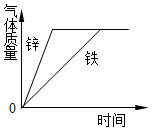 形状和质量相同的铁和锌分别加入到足量的同一种稀硫酸中 | |
| B. | 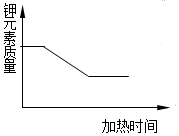 加热一定质量氯酸钾和二氧化锰混合固体 | |
| C. | 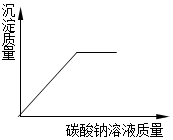 CaCl2和HCl混合液中加碳酸钠钠溶液 | |
| D. | 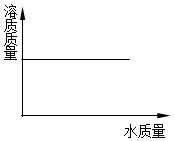 饱和KNO3溶液加水稀释 |
4.下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是( )
| A. | 闻气味 | B. | 观察颜色 | ||
| C. | 将集气瓶倒扣在水中 | D. | 将燃着的木条伸入集气瓶中 |
1.除去下列物质中的少量杂质(括号内为杂质),所用试剂及操作均正确的是( )
| A. | FeCl2溶液(CuCl2):加入过量铁粉、过滤 | |
| B. | 氯化钙溶液(盐酸):加入适量碳酸钠粉末 | |
| C. | NaOH溶液(Na2CO3):加入过量氧化钙、过滤 | |
| D. | CO2(HCl):通过足量氢氧化钠溶液 |
18.甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )
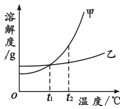

| A. | 依据溶解度曲线可判断,甲的溶解度比乙的大 | |
| B. | 将t2℃时甲的饱和溶液变为不饱和溶液,可采取升温或加水的方法 | |
| C. | t1℃时,甲、乙两溶液的溶质质量分数一定相等 | |
| D. | 将甲在t1℃的饱和溶液升温至t2℃,溶液的溶质质量分数增大 |
2. 为提高煤的利用率,减少污染,可将其转化成可燃性气体,此过程可以认为是碳与水的反应.其微观示意图如图所示,下列说法错误的是( )
为提高煤的利用率,减少污染,可将其转化成可燃性气体,此过程可以认为是碳与水的反应.其微观示意图如图所示,下列说法错误的是( )
 为提高煤的利用率,减少污染,可将其转化成可燃性气体,此过程可以认为是碳与水的反应.其微观示意图如图所示,下列说法错误的是( )
为提高煤的利用率,减少污染,可将其转化成可燃性气体,此过程可以认为是碳与水的反应.其微观示意图如图所示,下列说法错误的是( )| A. | 在化学变化中原子不可分 | B. | 生成物的分子个数比为1:1 | ||
| C. | 分子是由原子结合而成的 | D. | 生成的两种物质都属于单质 |
3.下列关于“酒精温度计遇冷读数下降”的微观解释正确的是( )
| A. | 分子停止运动 | B. | 分子间间隔减小 | ||
| C. | 分子体积缩小 | D. | 分子种类发生了变化 |