题目内容
13.氟氯代烷(商品名为氟利昂)在历史上是有名的制冷剂,它是在一定条件下用氟、氯原子取代CH4中的氢原子制得,如CF2Cl2、CFCl3等都属于氟氯代烷.在20世纪七八十年代科学家认识到氟氯代烷是破坏地球生命的“保护神”--高空臭氧层的主要物质,氟氯代烷上升到高空后,在紫外线的照射下分解出氯原子,参与破坏臭氧的反应:①Cl+O3=ClO+O2;②O3$\frac{\underline{\;紫外线\;}}{\;}$O2+O;③ClO+O=Cl+O2;
总反应:2O3=3O2.
请回答下列问题:
(1)反应结果是O3变成了O2,Cl在其中起催化作用.
(2)已知:氟氯代烷破坏臭氧的能力与化合物中氯元素的质量分数成正比.请分析氟氯代烷破坏臭氧的能力:CFCl3>CF2Cl2(填“>”、“=”或“<”)
分析 (1)根据催化剂的概念分析;
(2)根据两种物质中氯元素的质量分数分析;
解答 解:总反应:2O3=3O2;
(1)根据题目中所给信息分析,Cl在反应前后质量和性质没有发生改变,在反应中作催化剂,起催化作用;
(2)根据二者的化学式分析,CFCl3中氯元素的质量分数为:$\frac{35.5×3}{12+19+35.5×3}$×100%=77.45%;CF2Cl2中氯元素的质量分数为:$\frac{35.5×2}{12+19×2+35.5×2}$×100%=58.68%,根据题意应填大于.
故答案为:2O3=3O2;(1)催化;(2)>.
点评 本题考查了催化剂的作用侧重于基础知识的考查,题目难度不大.

练习册系列答案
相关题目
1.亲历化学实验话动,可以激发我们学习化学的兴趣,也可以让我们体验探究的过程.请你参与下列实验活.
【实验名称】探究燃烧的条件
【实聢目的】加深对燃烧条件的认识,体验实验探究的过程.
【实验用品】烧杯、玻璃棒,镊子,酒精灯,三脚架、大理石块,铜片,盐酸,酒精,棉花、乒乓球碎片、蜡烛、滤纸
【实验内容】请完成下表内容.
【实验名称】探究燃烧的条件
【实聢目的】加深对燃烧条件的认识,体验实验探究的过程.
【实验用品】烧杯、玻璃棒,镊子,酒精灯,三脚架、大理石块,铜片,盐酸,酒精,棉花、乒乓球碎片、蜡烛、滤纸
【实验内容】请完成下表内容.
| 实验序号 | 实验步骤 | 实验现象 | 实验结论 |
| (1) | 燃烧条件之一:需要可燃物 | ||
| (2) | 燃烧条件之二: | ||
| (3) | 燃烧条件之三: |
 钢铁被誉为现代工业的筋骨,是应用最广泛的金属材料.
钢铁被誉为现代工业的筋骨,是应用最广泛的金属材料. 无土栽培是现代农业栽培植物的一种方法.无土栽培的植物从营养液中吸取养料和水分.
无土栽培是现代农业栽培植物的一种方法.无土栽培的植物从营养液中吸取养料和水分.

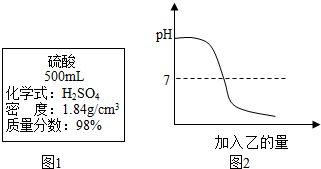 硫酸是重要的化工原料,也是实验室常用的酸.
硫酸是重要的化工原料,也是实验室常用的酸.