题目内容
15.小敏用氯酸钾和二氧化锰的混合物共29.5克来制取氧气,加热到不在产生气体时,冷却至室温后,称量剩余固体的质量为19.9克.请问 ①最多可以产生9.6克氧气;
②原混合物中有多少克氯酸钾?
分析 根据质量守恒定律可知固体反应前后的质量差为生成的氧气的质量,所以可以根据氧气的质量和对应的化学方程式求算原混合物中氯酸钾的质量
解答 解:根据质量守恒定律,生成的氧气的质量为29.5g-19.9g=9.6g
设生成9.6g的氧气需要的氯酸钾的质量为x.
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 9.6g
$\frac{245}{96}$=$\frac{x}{9.6g}$
x=24.5g
答:①最多可以产生9.6g氧气;
②原混合物中有24.5克氯酸钾.
点评 根据质量守恒定律计算最关键确定数据的有效性,进而根据对应的化学方程式求算对应的数据,注意过程的完整性和数据的准确性.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
6.NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl是著名的“侯氏制碱法”的重要反应.下列关于该反应的说法正确的是( )
| A. | NaHCO3是纯碱 | |
| B. | 往氯化铵溶液中加氯化钠,搅拌可以加大其溶解度 | |
| C. | 该条件下NaHCO3的溶解度较小 | |
| D. | 析出NaHCO3晶体后的溶液是NaHCO3的不饱和溶液 |
7.下列属于分子式的是( )
| A. | Cu | B. | Si | C. | CO2 | D. | NaCl |
4.中国科学家屠呦呦利用乙醚从黄花蒿汁液中提取出抗疟特效药青蒿素,从而获得了2015年诺贝尔医学奖.已知青蒿素的化学式为C15H22O5,其分子中含有与H2O2类似的结构,下列叙述正确的是( )
| A. | 青蒿素由碳、氢、氧原子构成 | B. | 1个青蒿素分子中含有11个氢分子 | ||
| C. | 提取青蒿素过程中应尽量避免高温 | D. | 青蒿素通过人工手段不能合成 |
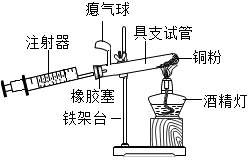 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为50mL的试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧试管口,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.请回答下列问题:
为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为50mL的试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧试管口,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.请回答下列问题: