题目内容
【题目】如图是部分元素的离子结构示意图和元素周期表的一部分。请回答:
| ||||||
| ||||||
|
| |||||
(1)图①、②中属于阴离子的是______(填序号),该元素的质子数为______;13号元素原子的最外层电子数为______。

(2)由表中原子序数为1、8、13的元素组成物质的化学式为______。
【答案】② 17 3 ![]()
【解析】
(1)图①的质子数为13,核外电子数为10,质子数>核外电子数,属于阳离子。图②的质子数为17,核外电子数为18,质子数<核外电子数,属于阴离子。第13号元素的核外电子的排布顺序为2、8、3。故答案为:②、17、3;
(2)原子序数为1、8、13的元素分别是氢元素、氧元素和铝元素,组成的物质是氢氧化铝,氢氧化铝中,铝元素化合价是+3,氢氧根化合价是-1,根据化合物中元素化合价代数和为零可知,氢氧化铝化学式是Al(OH)3。故答案为:Al(OH)3。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
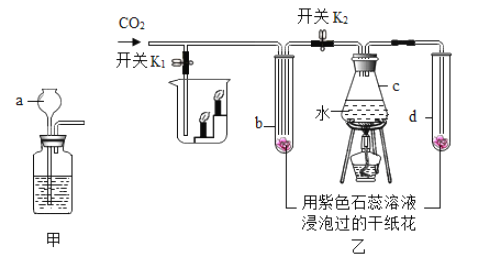
小学生10分钟应用题系列答案【题目】.某化学兴趣小组的同学研究CO2通入NaOH溶液是否发生反应,他们设计了以下实验。请你参与他们的探究活动,并回答有关问题。
(设计与实验)
实验序号 | 步骤一 | 步骤二 |
实验Ⅰ |
|
|
实验Ⅱ |
|
|
(探究与结论)
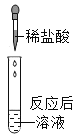
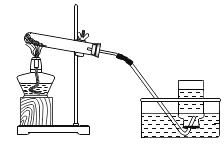
(1)实验I的步骤二中产生的实验现象是_________,反应的化学方程式为_______________。
(2)实验Ⅱ的步骤二中产生的实验现象是_____________。
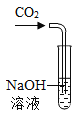
(3)在实验I、实验Ⅱ的步骤一中,CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是______________。
(拓展延伸)已知20℃时NaOH、Na2CO3在水中和酒精中的溶解度如下:
在水中的溶解度/g | 在酒精中的溶解度/g | |
NaOH | 109 | 17.3 |
Na2CO3 | 21.8 | <0.01 |
请利用以上信息设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。
(1)用化学方程式表示实验Ⅲ的原理:____________________。
(2)实验Ⅲ的主要操作是_____________________。
(交流反思)通过实验I~Ⅲ可知,验证无明显现象的反应是否发生,可以采用检验生成物的方法。请你再列举一种检验方法:______。