题目内容
2.请用数字和化学符号表示:(1)3个氮原子3N;
(2)2个碳酸分子2H2CO3;
(3)氧化镁中镁元素的化合价为+2价$\stackrel{+2}{Mg}$O;
(4)铵根离子NH4+;
(5)硫酸铁Fe2(SO4)3;
(6)2个氢氧根离子2OH-.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以3个氮原子,就可表示为:3N;
(2)分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以2个碳酸分子可表示为2H2CO3;
(3)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以氧化镁中镁元素的化合价为+2价,故可表示为:$\stackrel{+2}{Mg}$O;
(4)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故铵根离子可表示为:NH4+;
(5)硫酸铁是由显+3价的铁元素和显-2价的硫酸根组成的,根据化合价原则,其化学式为:Fe2(SO4)3;
(6)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个氢氧根离子可表示为:2OH-;
故答案为:(1)3N(2)2H2CO3(3)$\stackrel{+2}{Mg}$O(4)NH4+(5)Fe2(SO4)3(6)2OH-
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

 在一只盛有稀硫酸的烧杯中漂浮着一块木块(如图)往烧杯中加入少量的某中固体物质后,木块浸没在液体中的体积变大(假设这些过程中溶液的体积变化忽略不计),则加入的固体物质可能是( )
在一只盛有稀硫酸的烧杯中漂浮着一块木块(如图)往烧杯中加入少量的某中固体物质后,木块浸没在液体中的体积变大(假设这些过程中溶液的体积变化忽略不计),则加入的固体物质可能是( )| A. | Na2CO3 | B. | Fe | C. | Ba(OH)2 | D. | CuO |

【查阅资料】:碳酸镁晶须受热分解,生成3种氧化物;
【实验步骤】①组装仪器,查装置的气密性;②准确称取3.45g MgCO3•nH2O放在B装置中,连接仪器;③打开弹簧夹,鼓入一段时间空气,称量B、C、D、E、F装置的质量;④关闭弹簧夹,打开分液漏斗活塞,缓缓滴入稀盐酸至无气泡产生为止;⑤打开弹簧夹,鼓入一段时间空气;
⑥准确称量B、C、D、E、F装置的质量(如表);
| B | C | D | E | F | |
| 反应前 | 122.0g | 250.0g | 300.0g | 350.0g | 330.0g |
| 反应后 | 120.6g | 250.2g | 301.0g | 350.1g | 332.0g |
【实验分析及数据处理】
(1)完善实验步骤:①查装置的气密性;⑤鼓入一段时间空气;
(2)请计算碳酸镁晶须中的n值.(要求有计算过程)
(3)A装置中盛放的溶液是NaOH(浓)溶液;
【实验反思】
(4)下列选项中,会造成实验结果偏大的是①⑤;偏小的是②③⑥;
①反应结束后,没有通空气;②滴入稀盐酸前,没有通空气;③没有A装置; ④D装置中NaOH溶液浓度过大;⑤稀盐酸滴加速率太快; ⑥没有C装置;
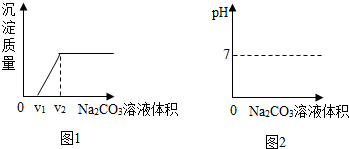
(5)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3•nH2O进行热重分析,并绘制出如图2所示的热重曲线示意图.则:
①0℃至t1℃时,剩余固体质量不变的原因为没有达到该晶分解需要的温度;
②t1℃至t2℃时MgCO3•nH2O分解的化学方程式为:MgCO3•3H2O═MgCO3•H2O+2H2O;
③完全反应后,剩余固体的质量m为4g.
| A. | CO和CO2的性质不同是因为分子的构成不同 | |
| B. | 在室内放一盆水可防止CO中毒 | |
| C. | 一氧化碳和二氧化碳都具有还原性 | |
| D. | 铅笔字迹易变模糊是因为常温下石墨化学性质活泼 |
(1)填表
| 实验步骤 | 观察到的现象 |
| A.在试管中取少量稀硫酸,插入足量的铁棒,充分作用. | ①产生气泡,溶液变成浅绿色 |
| B.在A所得的溶液中插入足量的②银棒,充分作用. | 无明显现象 |
| C.在B所得的溶液中插入足量的③铝棒,充分作用. | 该金属棒上附着黑色物质,溶液由浅绿色变为无色 |
(2)将锌棒插入前用砂纸打磨的原因是除去锌棒表面的氧化锌保护膜.
(3)小军同学认为在小琳设计的方案中,只要补充一个实验,就可得出Zn>Fe>H>Ag的结论.小军要补充的实验是把银棒插入稀硫酸中.
(4)现要得到Zn>Fe>H>Ag的结论.小楠同学认为不必做补充实验,只需将小琳同学方案中插入金属的顺序调整即可.你认为调整后依次插入金属棒的先后顺序为Ag、Fe、Al.
| A. | 用肥皂水检验软水和硬水 | |
| B. | 用带火星的木条区分空气、氧气和二氧化碳 | |
| C. | 除去一氧化碳中少量的二氧化碳,将气体通入足量的澄清石灰水 | |
| D. | 除去二氧化碳中少量的一氧化碳,将气体通过灼热的氧化铜 |
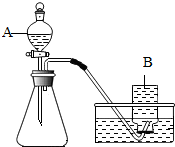 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.