题目内容
5.现有16g Fe2O3和CuO的混合粉末,把该混合物全部加入到100g足量的稀硫酸中,固体粉末完全溶解.然后滴加150g16%的氢氧化钠溶液,恰好完全反应,过滤.试计算:(1)所得滤液中的溶质是Na2SO4(写化学式),质量为42.6g.
(2)所用稀硫酸溶质的质量分数.
分析 Fe2O3和CuO的混合粉末,把该混合物全部加入到100g足量的稀硫酸,固体粉末完全溶解,溶液中溶质为硫酸铜、硫酸铁和硫酸,滴加150g16%的氢氧化钠溶液,恰好完全反应,过滤后转化为硫酸钠.找出Na+和SO42-之间的关系,由于无论开始怎么反应,最后加入氢氧化钠以后,都是钠离子和硫酸根离子结合为硫酸钠,所以有H2SO4~2NaOH~Na2SO4,然后根据这一关系解题即可.
解答 解:Fe2O3和CuO的混合粉末,把该混合物全部加入到100g足量的稀硫酸,固体粉末完全溶解,溶液中溶质为硫酸铜、硫酸铁和硫酸,滴加150g16%的氢氧化钠溶液,恰好完全反应,过滤后转化为硫酸钠.根据反应的方程式可得
设100g硫酸溶液中H2SO4的质量为x,生成Na2SO4的质量为y,由Na+和SO42-之间的关系得:
H2SO4~2NaOH~Na2SO4
98 80 142
x 150g×16% y
$\frac{98}{x}=\frac{80}{150g×16%}=\frac{142}{y}$;
x=29.4g,y=42.6g,
所以ω(H2SO4)=$\frac{29.4g}{100g}$×100%=29.4%,
答:(1)所得滤液中的溶质是Na2SO4,质量为42.6g,(2)硫酸溶液溶质的质量分数为29.4%.
点评 本题考查的是有关于溶质质量分数的简单计算的题目,在解题时,关键是找出隐含在题目中的解题条件Na+和SO42-之间的关系.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
20.用加热氯酸钾制取氧气时,加入一定量二氧化锰,这是为了( )
| A. | 制取更多的氧气 | B. | 使氯酸钾又快又多地生成氧气 | ||
| C. | 防止装置爆炸 | D. | 使氯酸钾低温下快速分解 |
17.下列方法不能使澄清石灰水变浑浊的是( )
| A. | 通入二氧化碳 | B. | 滴加碳酸钠 | C. | 放入CaO | D. | 放入KNO3 |
14.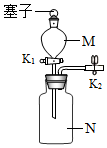 如图是实验室常用的一个装置,下列说法错误的是( )
如图是实验室常用的一个装置,下列说法错误的是( )
 如图是实验室常用的一个装置,下列说法错误的是( )
如图是实验室常用的一个装置,下列说法错误的是( )| A. | K2关闭、K1打开、塞子塞紧时,若M中的水不能流下则装置气密性好 | |
| B. | M中盛放双氧水,N中盛放二氧化锰,可以制取氧气 | |
| C. | M中盛放稀盐酸,N中盛放块状大理石,可以制取二氧化碳 | |
| D. | N中储满气体时,将水不断由M注入N中,即可将气体排出 |

