题目内容
4.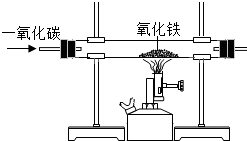 某同学设计了用一氧化碳与氧化铁反应来探究炼铁原理的装置,如图.
某同学设计了用一氧化碳与氧化铁反应来探究炼铁原理的装置,如图.(1)实验时先通入一会儿一氧化碳再加热,其目的是为了防止爆炸;从环保角度上看,上述装置有不足之处,改进措施是在装置尾部放置燃着的酒精灯.
(2)玻璃管中发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)铁架台是由铁合金制成的.铁的合金包括生铁和钢,二者含碳量较高的是生铁;铁架台的防锈措施是刷漆(写一点即可).
分析 (1)根据一氧化碳具有可燃性,容易发生爆炸;一氧化碳有毒不能直接排放到空气中考虑;
(2)根据实验现象的描述和方程式的书写方法考虑;
(3)根据生铁和钢的含碳量及铁制品的防锈措施分析解答.
解答 解:(1)因为一氧化碳具有可燃性,能和氧气混合在点燃的条件下会发生爆炸,所以实验开始时应先通一氧化碳再加热,目的是赶尽玻璃管内的空气,防止加热爆炸;一氧化碳有毒不能直接排放到空气中考虑,要点燃或收集;
(2)氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,所以现象是红色固体变为黑色,反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,根据得失氧进行配平,反应条件是高温,所以方程式是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)生铁含碳量在2%-4.3%之间,钢的含碳量0.03%-2%之间,所以生铁的含碳量高;铁生锈是铁和空气中的水分和氧气发生反应生成铁的氧化物,所以
隔绝空气或水分即可防锈.
故答案为:(1)爆炸;在装置尾部放置燃着的酒精灯;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(3)生铁;刷漆.
点评 解答本题关键是掌握方程式的书写要点和知道炼铁的注意事项.

练习册系列答案
相关题目
14.在一个密闭的容器内,有甲、乙、丙、丁四种物质,一定条件下发生化学反应,测得反应前后各物质的质量如下:
(1)分析表中数据可知,x=24g,该化学反应中可能是催化剂的物质为丙.
(2)该反应中甲与乙之间反应的质量比为5:2.
(3)写一个与该反应基本类型相同的化学方程式:CO2+H2O═H2CO3.
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 25 | 2 | 30 |
| 反应后质量(g) | 30 | 21 | 2 | X |
(2)该反应中甲与乙之间反应的质量比为5:2.
(3)写一个与该反应基本类型相同的化学方程式:CO2+H2O═H2CO3.
15.5月3日,在德国亥姆霍兹重离子研究中心,欧洲、美国、印度、澳大利亚和日本等多国研究人员在粒子加速器中,用钙离子轰击放射性元素锫,成功生成117号元素.117号元素很快又衰变成115号元素和113号元素.关于113号、115号、117号元素的最本质的区别是( )
| A. | 质子数不同 | B. | 中子数不同 | ||
| C. | 电子数不同 | D. | 相对原子质量不同 |
12.下列有关实验现象的描述正确的是( )
| A. | 甲烷燃烧生成二氧化碳和水 | B. | 磷在空气中燃烧产生大量白雾 | ||
| C. | 硫在氧气中燃烧产生淡监色火焰 | D. | 镁在空气中燃烧发出耀眼白光 |
9.甲、乙、丙、丁四个化学课外兴趣小组同学分别对各自实验废液中成分进行分析检测,结果如表;检测结果合理的是( )
| 检测小组 | 检测结果 |
| 甲组 | KCl、FeCl3、KOH、HCl |
| 乙组 | NaCl、Ca(NO3)2、K2CO3、HCl |
| 丙组 | NaCl、Mg(NO3)2、K2SO4、H2SO4 |
| 丁组 | KCl、KNO3、K2CO3、KOH |
| A. | 甲组、乙组 | B. | 丙组、丁组 | C. | 甲组、丙组 | D. | 乙组、丁组 |
 A~D是初中化学常见的物质,它们存在如下图所示的关系(“-”表示两物质间能反应,“→”表示一种物质转化成另一种物质.部分反应物和生成物及反应条件已略去).A、B、C是二种不同类别的含钙化合物,B常用作食品干燥剂.请回答下列问题.
A~D是初中化学常见的物质,它们存在如下图所示的关系(“-”表示两物质间能反应,“→”表示一种物质转化成另一种物质.部分反应物和生成物及反应条件已略去).A、B、C是二种不同类别的含钙化合物,B常用作食品干燥剂.请回答下列问题. 现有7g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的质量与加入的稀盐酸的质量关系如图所示.(友情提示:石灰石样品中的杂质不溶于水,也不发生反应,该反应的化学方程式为:
现有7g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的质量与加入的稀盐酸的质量关系如图所示.(友情提示:石灰石样品中的杂质不溶于水,也不发生反应,该反应的化学方程式为: