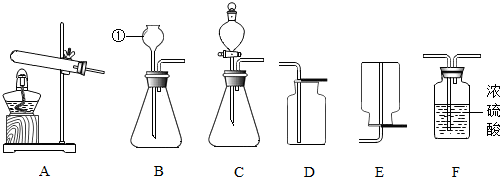
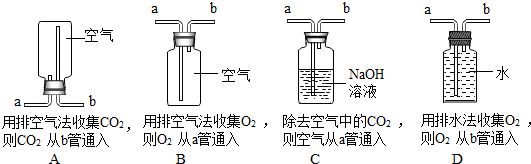
题目内容
3.交警对涉嫌酒驾的司机进行检测时,一般利用如下化学反应原理:C2H5OH+4CrO3(橙红色)+6H2SO4═2X(绿色)+9H2O+2CO2↑,则物质X的化学式为( )
| A. | Cr2(SO4)3 | B. | CrSO4 | C. | Cr2O3 | D. | CrSO3 |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:根据反应的化学方程式C2H5OH+4CrO3+6H2SO4═2X+2CO2↑+9H2O,反应物中碳、氢、氧(原子团之外的)、铬、硫酸根的个数分别为2、18、13、4、6,反应后的生成物中碳、氢、氧、铬、硫酸根原子的个数分别为2、18、13、0、0,根据反应前后原子种类、数目不变,则2X中含有4个铬原子、6个硫酸根,则每个X分子由2个铬原子和3个硫酸根构成,则物质X的化学式为Cr2(SO4)3.
故选A.
点评 本题难度不大,利用化学反应前后元素守恒、原子守恒来确定物质的化学式是解题的关键.

练习册系列答案
相关题目
5.化学在工农业生产、科技发展和社会生活中发挥着重要作用,下列说法不正确的是( )
| A. | 用铝合金制飞机外壳是因其硬度大、密度小、耐腐蚀 | |
| B. | 无土栽培的营养液中常含的K2SO4是一种复合肥 | |
| C. | 发射火箭采用的液氢、液氧都是无污染的纯净物 | |
| D. | 生活中常用加热煮沸的方法降低水的硬度 |
6.下列图标表示我国“国家节水标志”的是( )
| A. |  | B. |  | C. |  | D. |  |
3.下列各组溶液,只用组内物质不能鉴别的是( )
| A. | NaN03 KCl Na2CO3 HCl | B. | HCl Na2CO3 K2SO4 BaCl2 | ||
| C. | MgSO4 KOH KNO3 CuSO4 | D. | KOH MgCl2 H2SO4 NaCl |
8.下列事实的结论或解释中不正确的是( )
| A. | 食物腐败-分子的种类改变 | |
| B. | 桂花开,满园香-分子在不断运动 | |
| C. | 碘升华-分子的体积变大了 | |
| D. | 反应前后质量守恒-原子种类、数目和质量没有改变 |
15.如图所示图象不能正确反映对应变化关系的是( )
| A. |  用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 | |
| B. |  向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液 | |
| C. |  将水通电电解,一段时间氢气和氧气的体积比 | |
| D. |  向两份完全相同的稀硫酸中分别加入锌粉、镁 |
12.某同学为探究某种铜铁合金中铁的质量分数,先后在烧杯中进行了四次试验(杂质不与稀硫酸反应),实验数据如下表:
根据该同学的实验,试回答以下问题:
(1)上表第四次实验中合金里的铁恰好与稀硫酸完全反应,则其中X=150,Y=179.4.
(2)该铜铁合金中铁的质量分数.
(3)所加稀硫酸溶质质量分数(结果保留至0.1%).
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 所取合金的质量/g | 10 | 10 | 20 | 30 |
| 所加稀硫酸的质量/g | 80 | 100 | 50 | X |
| 反应后烧杯中剩余物质的质量/g | 89.8 | 109.8 | 69.8 | Y |
(1)上表第四次实验中合金里的铁恰好与稀硫酸完全反应,则其中X=150,Y=179.4.
(2)该铜铁合金中铁的质量分数.
(3)所加稀硫酸溶质质量分数(结果保留至0.1%).