题目内容
16.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤,不可能存在的情况是( )①滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+
②滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Mg2+
③滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
④滤纸上有Ag、Cu、Zn、Mg,滤液中有Zn2+、Mg2+.
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
分析 镁比锌活泼,锌比铜活泼,铜比银活泼,根据具体的反应情况可以进行相关方面的判断.
解答 解:如果锌不足以硝酸银完全反应,则滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+;
如果滤纸上有Ag、Cu,说明硝酸银已经完全反应,则滤液中不可能有Ag+;
如果锌过量,则滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+;
因为镁比锌活泼,因此锌不能和硝酸镁反应,即滤纸上不可能有镁;
由分析可知,②④的情况不可能存在.
故选:D.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
11.下列各组变化中,前者是物理变化,后者是化学变化的是( )
| A. | 蜡烛熔化,蜡烛燃烧 | B. | 水变成水蒸气,水结成冰 | ||
| C. | 铁矿石炼铁,铁器生锈 | D. | 汽油挥发,汽油燃烧 |
5.下列说法正确的是( )
| A. | 用甲醛溶液浸泡海产品保鲜 | |
| B. | 用氢氧化钠溶液去除氧气中少量水蒸气 | |
| C. | 熟石灰能与稀盐酸反应,因此熟石灰用于治疗胃酸过多 | |
| D. | 鉴别羊毛与合成纤维,在空气中点燃,闻产生的气味 |
6.下列方案合理的是( )
| A. | 验证碱能与酸反应:将H2SO4溶液滴入Cu(OH)2中 | |
| B. | 检验碳酸根离子:将要检验的物质与稀盐酸混合,观察是否产生气泡 | |
| C. | 验证质量守恒定律:将锌粒与稀硫酸混合,比较混合前后溶液的质量 | |
| D. | 鉴别H2、CH4、CO三种气体:分别将燃着的木条伸入集气瓶内,观察现象 |
 (1)所标物质中属于金属单质的是Cu;
(1)所标物质中属于金属单质的是Cu;
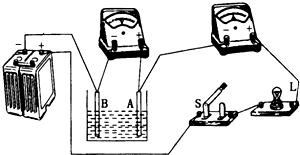 如图所示,A、B为两个电极,放在盛有稀硫酸的玻璃容器内.闭合开关后,A电极上出现的气泡为氧气,B电极上出现的气泡为氢气,在这一过程中,电流表示数逐渐变变大;灯泡亮度逐渐变亮.
如图所示,A、B为两个电极,放在盛有稀硫酸的玻璃容器内.闭合开关后,A电极上出现的气泡为氧气,B电极上出现的气泡为氢气,在这一过程中,电流表示数逐渐变变大;灯泡亮度逐渐变亮.