题目内容
下列实验方案的设计合理的是( )
| 序号 | 实验目的 | 实验方案 |
| A | 区分NaCl溶液和CaCl2溶液 | 取样,通入CO2 |
| B | 制FeSO4溶液 | 氧化铁和稀硫酸反应 |
| C | 检验NaOH溶液是否变质 | 取样,滴加BaCl2溶液 |
| D | 除去Cu中的CuO | 加足量稀硫酸、过滤、蒸发 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案设计与评价,酸的化学性质,碱的化学性质,盐的化学性质,酸、碱、盐的鉴别
专题:简单实验方案的设计与评价
分析:A、首先对需要鉴别的物质的性质进行对比分析找出特性,再根据性质的不同,选择适当的试剂,出现不同的现象的才能鉴别.
B、根据氧化铁和稀硫酸反应生成硫酸铁和水,进行分析判断.
C、氢氧化钠溶液变质后生成的杂质是碳酸钠,因此检验是否变质即检验是否存在碳酸根离子.
D、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
B、根据氧化铁和稀硫酸反应生成硫酸铁和水,进行分析判断.
C、氢氧化钠溶液变质后生成的杂质是碳酸钠,因此检验是否变质即检验是否存在碳酸根离子.
D、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:A、二氧化碳均不能与NaCl溶液和CaCl2溶液反应,不能出现两种明显不同的现象,不能鉴别,故实验方案的设计不合理.
B、氧化铁和稀硫酸反应生成硫酸铁和水,不能制FeSO4溶液,故实验方案的设计不合理.
C、氢氧化钠溶液变质后生成的杂质是碳酸钠,氢氧化钠与氯化钡溶液不反应,碳酸钠能与BaCl2溶液反应生成碳酸钡沉淀和氯化钠,可根据是否有沉淀生成检验NaOH溶液是否变质,故实验方案的设计合理.
D、CuO能与稀硫酸反应生成硫酸铜和水,铜不与稀硫酸反应,再过滤、洗涤、干燥,故实验方案的设计不合理.
故选:C.
B、氧化铁和稀硫酸反应生成硫酸铁和水,不能制FeSO4溶液,故实验方案的设计不合理.
C、氢氧化钠溶液变质后生成的杂质是碳酸钠,氢氧化钠与氯化钡溶液不反应,碳酸钠能与BaCl2溶液反应生成碳酸钡沉淀和氯化钠,可根据是否有沉淀生成检验NaOH溶液是否变质,故实验方案的设计合理.
D、CuO能与稀硫酸反应生成硫酸铜和水,铜不与稀硫酸反应,再过滤、洗涤、干燥,故实验方案的设计不合理.
故选:C.
点评:本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
下列关于氧气的化学性质的叙述中,正确的是( )
| A、氧气和硫反应生成无色无味的气体 |
| B、氧气和碳反应生成白色的固体 |
| C、红热的铁丝在氧气中剧烈燃烧,生成黑色的固体 |
| D、红磷在氧气中燃烧,产生大量的白雾 |
食醋中通常含有3%-5%的醋酸,则下列关于食醋的用途不正确的是( )
| A、吃松花蛋时蘸醋可消除涩味 |
| B、可用于清除去水垢 |
| C、儿童误食生石灰时可喝醋缓解 |
| D、治疗胃酸过多 |
在一个密闭容器中放入W、G、H、P四种物质,在一定条件下充分反应,一段时间后,测得有关数据如下表,对此反应的认识不正确的是( )
| 物质 | W | G | H | P |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | 待测 | 26 | 2 | 12 |
| A、物质H可能是反应的催化剂 |
| B、该反应可能属于分解反应 |
| C、在生成物和反应物中,G、P的质量比为5:4 |
| D、待测值为13 |
下列物质的化学式书写正确的是( )
| A、氢氧化钙CaOH |
| B、氧化铁FeO |
| C、氯化钠NaCl |
| D、氧化铜CuO2 |
由于药品本身的腐蚀性可能对人体伤害的药品是( )
| A、甲醇 | B、一氧化碳 |
| C、烧碱 | D、硫酸铜 |
下列实验操作中,不正确的是( )
A、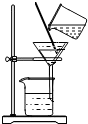 过滤 |
B、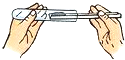 取固体粉末 取固体粉末 |
C、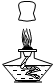 熄灭酒精灯 |
D、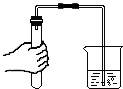 检查气密性 检查气密性 |