题目内容
7. 眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图:
眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图:(1)所标物质中属于金属单质的是铜螺丝,属于有机合成材料的是塑料脚套.
(2)夏天铜螺丝部位常出现一层绿色物质,这是由于铜生锈的原因,请完成该反应的化学方程式:2Cu+O2+CO2+H2O=Cu2(OH)2CO3,此反应属于基本类型中的化合反应.
(3)该款变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜.在强光照射下,溴化银分解成溴(Br2)和银,玻璃颜色变深,请完成该反应的化学方程式:2AgBr$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{氧化铜}$2Ag+Br2.当光线变暗时,溴和银在氧化铜作用下,重新生成溴化银,玻璃颜色变浅,氧化铜在反应中起催化作用.
分析 (1)根据材料的分类知识进行分析;
(2)由质量守恒定律和方程式的书写规则进行书写,以及根据反应类型的特点判断反应类型;
(3)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;溴单质和银在氧化铜作用下,能够重新生成溴化银,说明氧化铜在反应中起到催化剂的作用.
解答 解:(1)铜螺丝属于金属单质,塑料脚套属于有机合成材料,故填:铜螺丝,塑料脚套;
(2)铜生锈是铜与空气中的水和二氧化碳起作用,反应的化学方程式为:2Cu+O2+CO2+H2O=Cu2(OH)2CO3;该反应符合多变一的特点,故属于化合反应
(3)在强光照射下,溴化银分解成溴单质和银的化学方程式为:2AgBr$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{氧化铜}$2Ag+Br2;
当光线变暗时,溴单质和银在氧化铜作用下,又重新生成溴化银,玻璃颜色变浅,氧化铜在该反应中起催化作用.
故答案为:(1)铜螺丝;塑料脚套;(2)2Cu+O2+CO2+H2O=Cu2(OH)2CO3;化合(3)2AgBr$\frac{\underline{\;\;\;\;\;光\;\;\;\;\;}}{氧化铜}$2Ag+Br2;催化.
点评 本题难度不大,利用化学反应前后元素守恒、原子守恒来确定物质的化学式以及掌握物质的分类等是正确解题的关键.

练习册系列答案
相关题目
17. 德国一著名车企与另一公司合作发展生质柴油.简要过程如图,蓝原油的成分与天然原油相似.下列有关说法不正确的是( )
德国一著名车企与另一公司合作发展生质柴油.简要过程如图,蓝原油的成分与天然原油相似.下列有关说法不正确的是( )
 德国一著名车企与另一公司合作发展生质柴油.简要过程如图,蓝原油的成分与天然原油相似.下列有关说法不正确的是( )
德国一著名车企与另一公司合作发展生质柴油.简要过程如图,蓝原油的成分与天然原油相似.下列有关说法不正确的是( )| A. | 三大化石燃料是指煤、石油和天然气 | |
| B. | 此过程中电解水装置中产生的氢气与氧气的体积比等于2:1 | |
| C. | 该方法获得的生物柴油如获得成功推广,温室效应将完全消除 | |
| D. | 氢能、风能、太阳能都属于绿色能源 |
18.生活离不开化学.下列说法错误的是( )
| A. | 活性炭能除去水中的异味 | |
| B. | 煤的使用给人类带来很多方便且不会对环境造成不良影响 | |
| C. | 吸烟有害健康 | |
| D. | 油锅着火可用锅盖盖灭 |
15.工业上用甲、乙制备化学肥料丙,同时有丁生成.根据下列微观示意图得出的结论中,正确的是( )

①甲的化学式为NH3 ②乙、丙、丁都是氧化物
③丙中氮、氢元素质量比为7:1 ④参加反应的甲、乙质量比为17:44.

①甲的化学式为NH3 ②乙、丙、丁都是氧化物
③丙中氮、氢元素质量比为7:1 ④参加反应的甲、乙质量比为17:44.
| A. | ① | B. | ①③ | C. | ①④ | D. | ② |
2.如图是模拟海水制盐的流程
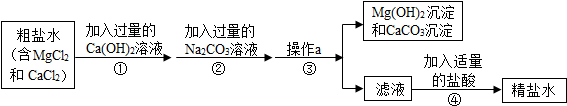
操作a的名称是过滤,所需要的玻璃仪器有漏斗(只写其中一种玻璃仪器).
【提出问题】滤液中除了含有氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠,所以滤液中除了含有氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有氯化钠外,还含有氢氧化钠和碳酸钠.
【验证猜想】
【反思与拓展】为了使制得的精盐水只含有氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:NaOH+HCl═NaCl+H2O.如果要将精盐水继续提纯成NaCl晶体,应进行蒸发结晶操作.
组成探究】
纯碱也是一种较为重要的基础化工原料,某才同学们为了测定某纯碱样品(混有少量氯化纳)的纯度,设计了如下实验:

根据实验数据,计算该纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)

操作a的名称是过滤,所需要的玻璃仪器有漏斗(只写其中一种玻璃仪器).
【提出问题】滤液中除了含有氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠,所以滤液中除了含有氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有氯化钠外,还含有氢氧化钠和碳酸钠.
【验证猜想】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量滤液于试管中,加入过量的氯化钙溶液,振荡,静置 | 产生白色沉淀 | 猜想三是正确的 |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入无色酚酞试液(填指示剂) | 溶液变红色 |
组成探究】
纯碱也是一种较为重要的基础化工原料,某才同学们为了测定某纯碱样品(混有少量氯化纳)的纯度,设计了如下实验:

根据实验数据,计算该纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)
12.下列化学用语书写正确的是( )
| A. | 银元素Hg | B. | 4个氢原子H4 | C. | 铵根离子NH4+ | D. | 氮分子N |
19.下列有关物质的检验、鉴别、除杂、分离所用的试剂或方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 检验一瓶气体是否为CO2 | 燃着的木条 |
| B | 鉴别氢氧化钠溶液和饱和石灰水 | 升高温度 |
| C | 分离铁粉和铜粉混合物 | 稀硫酸 |
| D | 除去NaOH溶液中的Na2CO3 | 氢氧化钙溶液 |
| A. | A | B. | B | C. | C | D. | D |
17.二氧化锰与含有的X溶液混合并加热,可以制取氯气,其化学方程式为MnO2+X$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,则下列说法正确的是( )
| A. | X中所含元素的质量比为1:1 | |
| B. | 二氧化锰在该反应中起催化作用 | |
| C. | 该反应的化学方程式中,X的化学计量数是4 | |
| D. | 反应前后Mn元素的化合价不变 |
