题目内容
4. 如图所示是甲、乙两种物质的溶解度曲线.将t2℃时等质量的甲、乙两种物质的饱和溶液降温到t1℃时( )
如图所示是甲、乙两种物质的溶解度曲线.将t2℃时等质量的甲、乙两种物质的饱和溶液降温到t1℃时( )| A. | 两种溶液仍是饱和溶液 | B. | 两种溶液的质量仍相同 | ||
| C. | 甲乙都会有晶体析出现 | D. | 乙溶液中溶剂的质量比甲多 |
分析 A、据甲、乙的溶解度随温度变化情况分析降温后溶液状态变化;
B、甲的溶解度随温度降低而减小,要析出晶体,溶液质量减小,乙的溶解度随温度降低而增大,溶液质量不变;
C、据二者溶解度随温度变化分析解答;
D、根据t2℃时二者的溶解度及溶液质量相等分析溶剂质量多少.
解答 解:A、乙的溶解度随温度降低而增大,所以降温后变为不饱和溶液,故错误;
B、甲的溶解度随温度降低而减小,要析出晶体,溶液质量减小,乙的溶解度随温度降低而增大,溶液质量不变,故错误;
C、由B可知,甲降温后溶质减小,析出晶体,乙溶解度减小,不会析出晶体,故错误;
D、t2℃时甲的溶解度大于乙 的溶解度,所以t2℃时等质量的甲、乙两种物质的饱和溶液中甲溶液中溶剂的质量比乙少,降温溶剂的质量不变,故正确;
故选:D.
点评 本题考查了溶解度曲线的意义,注重考查学生对知识的掌握和应用能力.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
12.根据质量守恒定律,3克碳和8克氧气充分反应后,生成二氧化碳的质量是( )
| A. | 13.75克 | B. | 13克 | C. | 11克 | D. | 7克 |
12.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 用生石灰制熟石灰 CaO+2H2O═Ca(OH)2 化合反应 | |
| B. | 用氯酸钾和二氧化锰制取氧气 2KClO3$\frac{\underline{MnO_2}}{△}$2Kl+3O2↑ 分解反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 用纯碱制烧碱 2KOH+Na2CO3=K2CO3+2NaOH 复分解反应 |
19.做化学实验时你一定留心观察过,在下列仪器中盛放固体药品的仪器是( )
| A. |  广口瓶 | B. |  细口瓶 | C. |  烧杯 | D. |  集气瓶 |
9.下列反应属于分解反应的是( )
| A. | 硫在氧气中燃烧 | B. | 氯酸钾和二氧化锰混合加热制氧气 | ||
| C. | 铁在氧气中燃烧 | D. | 蜡烛燃烧 |
16.某同学在学习了燃烧与燃料的有关知识后,注意到一张纸容易燃烧,而卷成纸团却不易燃烧,联想到细铁丝受热后,在空气中一般只产生红热现象,而在氧气中能剧烈燃烧,于是引发思考,并进行了实验探究.请你协助回答下面有关问题:
【发现问题】:可燃物燃烧的剧烈程度与哪些因素有关呢?
【提出猜想】:猜想①:燃烧的剧烈程度可能与氧气的浓度有关;猜想②:燃烧的剧烈程度可能与可燃物与氧气的接触面积有关.
【验证猜想】:实验报告如下:
【发现问题】:可燃物燃烧的剧烈程度与哪些因素有关呢?
【提出猜想】:猜想①:燃烧的剧烈程度可能与氧气的浓度有关;猜想②:燃烧的剧烈程度可能与可燃物与氧气的接触面积有关.
【验证猜想】:实验报告如下:
| 验证猜想 | 实验操作 | 实验现象 | 实验结论 |
猜想① | 燃烧更剧烈 | ||
猜想② | 燃烧更剧烈 |
13.将10g NaOH溶解在100g水中,所得溶液不饱和,该溶液中溶质的质量分数为( )
| A. | 11% | B. | 10% | C. | 9.1% | D. | 1% |
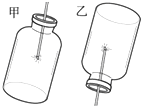 装满氧气的集气瓶,如图所示,当用带火星的木条分别以甲、乙两种方式迅速插入瓶中,木条复燃,而且在甲中燃烧比乙中更旺更持久.上述实验证明氧气具有的性质是氧气能支持燃烧;氧气的密度比空气的大.
装满氧气的集气瓶,如图所示,当用带火星的木条分别以甲、乙两种方式迅速插入瓶中,木条复燃,而且在甲中燃烧比乙中更旺更持久.上述实验证明氧气具有的性质是氧气能支持燃烧;氧气的密度比空气的大.