题目内容
1.在化学反应2A+B═2C+D中,若A的式量为80,B的式量为12,D的式量为44,则C的式量为64.分析 解答此题需依据质量守恒定律,反应前后质量总和相等,所以参加反应的A和B的质量和等于生成物C和D的质量和,以此为突破口,找出D的质量,再根据D的相对分子质量,可以求得C的相对分子质量.根据反应物和生成物中各物质之间的质量比,等于它们相对分子质量总和之比,即可解答;
解答 解:根据质量守恒定律可知,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.因为“在化学反应2A+B═2C+D中,若A的式量为80,B的式量为12,D的式量为44”,则2×80+12=2C+44,解得C=64.
故答案为:64.
点评 本题综合考查了质量守恒定律的应用和化学方程式表示的含义.反应物和生成物中各物质的相对分子质量总和之比,等于它们之间的质量比.

练习册系列答案
相关题目
9.向氯化钠的饱和溶液中再加入氯化钠晶体,则溶液中( )
| A. | 溶质质量分数不变 | B. | 溶液质量变大 | ||
| C. | 溶剂质量变小 | D. | 溶质质量分数变大 |
16.下列变化中,属于分解反应的是( )
| A. | 碳十氧气$\stackrel{点燃}{→}$二氧化碳 | B. | 水$\stackrel{通电}{→}$氢气十氧气 | ||
| C. | 酒精十氧气$\stackrel{点燃}{→}$二氧化碳十水 | D. | 氢气十氧气$\stackrel{点燃}{→}$水 |
10.化学实验小组的同学取一定量的Ca(OH)2溶液与Na2CO3溶液混合,充分反应后过滤,得到无色滤液,他们对滤液的成分进行了实验探究.
(1)如果滤液中只含一种溶质,则该溶质是NaOH,写出生成该物质的化学方程式Ca(OH)2+Na2CO3═CaCO3+↓2NaOH,并请设计实验方案进行确认,填写实验报告.
(1)如果滤液中只含一种溶质,则该溶质是NaOH,写出生成该物质的化学方程式Ca(OH)2+Na2CO3═CaCO3+↓2NaOH,并请设计实验方案进行确认,填写实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取少量滤液于一支试管中,向其中一支加入少量稀盐酸向其中一支加入少量稀盐酸,振荡 | 无明显变化 | 滤液中没有Na2CO3 |
| 2.在另一支试管中再加入少量滤液,向其中加入少量Na2CO3. | 无明显变化 | 滤液中没有Ca(OH)2. |
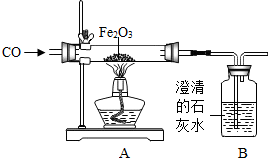 化学兴趣小组的同学设计了用一氧化碳气体还原氧化铁的实验装置,如图所示.请回答下列问题:
化学兴趣小组的同学设计了用一氧化碳气体还原氧化铁的实验装置,如图所示.请回答下列问题: 有三种常见的物质A、B和C,它们之间的相互转化关系如图所示.已知,A、C在常温常压下都是由两种相同的元素组成的无色液体,B是空气的组成成分之一.请按要求填空:
有三种常见的物质A、B和C,它们之间的相互转化关系如图所示.已知,A、C在常温常压下都是由两种相同的元素组成的无色液体,B是空气的组成成分之一.请按要求填空: