题目内容
6.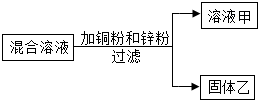 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.(1)向固体乙上滴加盐酸时没有(填“有”或“没有”)气泡产生.
(2)溶液甲中一定含有哪些溶质?(写化学式)Zn(NO3)2、Cu(NO3)2、Al(NO3)3.
(3)请写出该实验过程中所发生反应的两个化学方程式.
分析 铝比锌活泼,锌比铜活泼,铜比银活泼,把铜和锌加入溶液中时,锌先和硝酸银反应生成硝酸锌和银,当锌完全反应后,铜再和硝酸银反应,甲溶液是蓝色的,说明铜和硝酸银发生了反应,进一步说明锌已经完全反应,向固体乙上滴加盐酸时没有气泡产生;
锌和硝酸银反应生成硝酸锌和银,铜和硝酸银反应生成硝酸铜和银.
解答 解:(1)铝比锌活泼,锌比铜活泼,铜比银活泼,把铜和锌加入溶液中时,锌先和硝酸银反应生成硝酸锌和银,当锌完全反应后,铜再和硝酸银反应,甲溶液是蓝色的,说明铜和硝酸银发生了反应,进一步说明锌已经完全反应,向固体乙上滴加盐酸时没有气泡产生;
故填:没有.
(2)溶液甲中一定含有硝酸锌、硝酸铜和硝酸铝,化学式分别是Zn(NO3)2、Cu(NO3)2、Al(NO3)3.
故填:Zn(NO3)2、Cu(NO3)2、Al(NO3)3.
(3)锌、铜和硝酸银反应的化学方程式分别为:Zn+2AgNO3=Zn(NO3)2+2Ag、Cu+2AgNO3=Cu(NO3)2+2Ag.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
16.如图表示一杯刚配制的饱和蔗糖溶液,要增加该溶液的溶质质量分数,下列操作正确的是( )


| A. | 降温 | B. | 升温 | C. | 加糖 | D. | 搅拌 |
17. 铕是一种稀土元素,常用作彩色电视机的荧光粉,在激光材料及原子能工业中有重要的应用.如图是元素周期表中铕元素的相关信息,下列说法不正确的是( )
铕是一种稀土元素,常用作彩色电视机的荧光粉,在激光材料及原子能工业中有重要的应用.如图是元素周期表中铕元素的相关信息,下列说法不正确的是( )
 铕是一种稀土元素,常用作彩色电视机的荧光粉,在激光材料及原子能工业中有重要的应用.如图是元素周期表中铕元素的相关信息,下列说法不正确的是( )
铕是一种稀土元素,常用作彩色电视机的荧光粉,在激光材料及原子能工业中有重要的应用.如图是元素周期表中铕元素的相关信息,下列说法不正确的是( )| A. | 铕属于非金属元素 | B. | 铕原子的质子数为63 | ||
| C. | 铕原子核外有63个电子 | D. | 铕的相对原子质量为152.0 |
11.下列化学现象的描述,错误的是( )
| A. | 氢氧化钠固体溶于水放热 | |
| B. | 红磷在空气中燃烧发出白光,生成大量的白色烟雾 | |
| C. | 分别蘸有浓盐酸与浓氨水的玻璃棒靠近产生白烟 | |
| D. | 硫在氧气中燃烧发出明亮的蓝紫色火焰,放热,生成一种有刺激性气味的气体 |
15. 部分含钙物质间的转化关系如图所示,下列分析正确的是( )
部分含钙物质间的转化关系如图所示,下列分析正确的是( )
 部分含钙物质间的转化关系如图所示,下列分析正确的是( )
部分含钙物质间的转化关系如图所示,下列分析正确的是( )| A. | CaO、Ca(OH)2、CaCO3都是含氧化合物,简称氧化物 | |
| B. | 转化①是氯化钙溶液中的钙被置换出来 | |
| C. | 转化④一定是中和反应 | |
| D. | 转化⑥可能是复分解反应 |