题目内容
14.在实验室选用如图中A-G的装置可以制取气体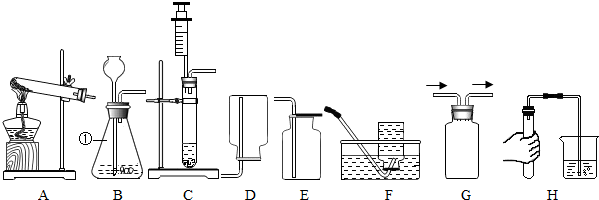
(1)用分子的观点解释H操作的现象温度升高气体分子间隔增大,体积增大,气体膨胀逸出,导管口有气泡产生.
(2)某同学选用装置A和F来制取氧气,请写出该方法制氧气的化学方程式2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室制二氧化碳气体可选用装置B和C,其中装置B中的长颈漏斗下端管口要浸在液面下,其目的是:形成液封,防止气体从管口逸出,与装置B相比,C装置的优点有:可以控制反应速率.
(4)实验室常用氯化铵固体与熟石灰固体共热来制取氨气.请写出该方法制取氨气发生反应的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水.请根据信息回答下列问题:
①实验室制取氨气可选用的装置是AD(填序号);
②若用如图G装置进行“排空气法”收集制取的NH3,请把图中的“导气管”补画完整.
分析 (1)根据温度越高气体分子运动速率加快,间距离增大,体积膨胀进行解答;
(2)根据实验室用氯酸钾制取氧气的反应原理书写方程式;
(3)装置B中长颈漏斗的作用是向装置内加液体,漏斗下端管口要伸入到液面以下的原因是形成液封,防止气体从管口逸出;装置C的优点是控制反应速率;
(4)据氯化铵和熟石灰反应原理书写方程式;
①实验室常用氯化铵固体与熟石灰固体共热来制取氨气,由于需要进行加热,属于固体加热型,故选发生装置A,据氨气的溶解性和密度选择收集装置;
②根据氨气的密度比空气小,应短进长出解答.
解答 解:
(1)H操作是检查装置的气密性装置,检验其气密性的方法是:用手握住广口瓶,若观察到烧杯中导气管口有气泡产生,说明气密性良好;该检测方法的依据是:分子间有间距,且分子间距随温度升高而增大,随温度的降低而减小;
(2)装置A是加热固体制取氧气,且试管口无棉花,说明是用加热氯酸钾的方法制取氧气,反应的化学方程式为:2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)装置B中长颈漏斗的作用是向装置内加液体,漏斗下端管口要伸入到液面以下的目的是形成液封,防止气体从管口逸出;装置C的优点是可用通过控制反应物的量,来控制反应速率;
(4)制取氨气的反应物是氯化铵与熟石灰,生成物是氯化钙、水、氨气,用观察法配平,氨气后面标上上升符号,反应条件是加热写在等号的上边,方程式是:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
①实验室常用氯化铵固体与熟石灰固体共热来制取氨气,由于需要进行加热,属于固体加热型,故选发生装置A;由于常温下NH3密度比空气小,可用向下排空气法收集;因其极易溶于水,则不能用排水法;故收集装置为D;
②若用如图G装置进行“排空气法”收集制取的氨气,氨气的密度比空气小,应短进长出,将空气挤压到集气瓶上部排出,图示为: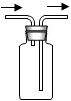
故答案为:
(1)温度升高气体分子间隔增大,体积增大,气体膨胀逸出,导管口有气泡产生;
(2)2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)形成液封,防止气体从管口逸出; 可以控制反应速率;
(4)2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
①A D;
②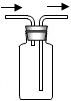
点评 本题主要考查了实验室中制取气体的反应原理,发生装置和收集装置选择的依据,及有关的知识,能较好培养学生分析、解答问题的能力.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案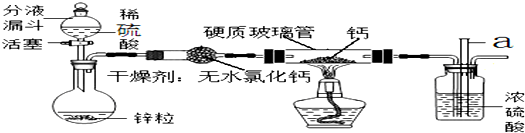
【提出问题】硬质玻璃管中的钙是否完全转化为CaH2?
【查阅资料】
(1)金属钙活动性很强,遇水反应生成氢化钙,同时产生一种气体;
(2)氢化钙要密封保存,遇水反应放出氢气.
【猜想与实验】
(1)固体为Ca和CaH2.
(2)固体为CaH2.
甲同学的探究活动如下:
| 实验操作 | 实验现象 | 实验结论及解释 |
| ①取少量硬质玻璃管中的固体于试管中,滴入少量水,收集产生的气体,并用燃着的木条点燃. | 冒气泡;气体燃烧,产生淡蓝色火焰 | 有氢气生成 |
| ②继续向溶液中滴加酚酞. | 呈红色 | 生成Ca(OH)2(填化学式) |
乙同学认为由以上探究活动还不能得出猜想1正确,理由是若固体为CaH2,遇水反应也会产生相同的现象,请你帮助乙设计实验,写出主要的实验步骤、现象和相应结论:取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积.若体积相等,说明玻璃管中Ca完全转化为CaH2;若不相等,则说明Ca未完全转化为CaH2.
【反思讨论】
(1)写出CaH2与水反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是便于携带、避免爆炸危险.
(3)制备CaH2装置中,玻璃管a的作用是检验装置的气密性.
| A. | 人工降雨的常用材料是干冰和碘化银 | |
| B. | 人工降雨的主要作用是使空气中的水蒸气发生凝结或凝华 | |
| C. | 人工降雨随时可以进行,只要人们需要 | |
| D. | 正在下落的雨滴具有机械能和内能 |
| A. | 冰 干冰 硫酸 | B. | 生铁 纯碱 石油 | ||
| C. | 水银 生石灰 天然气 | D. | 石墨 氯酸钾 空气 |
| A. | 液态水变成水蒸气时,水分子变大 | |
| B. | 过滤和加热均能使硬水转化为软水 | |
| C. | 蒸馏或用活性炭吸附均可使海水转化为淡水 | |
| D. | 电解水时负极和正极生成气体的质量比为1:8 |
| A. | 盐酸 | B. | 硫酸 | C. | 硫酸钠 | D. | 石蕊试剂 |
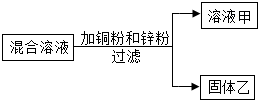 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.