题目内容
3.现有用稀盐酸和酚酞混合液浸过的滤纸,分别在滤纸上滴加下列溶液,则滤纸上不会出现红色的是( )| A. | 硫酸 | B. | 石蕊试液 | C. | 澄清石灰水 | D. | KOH溶液 |
分析 根酸的化学性质,紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝;无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红;进行分析解答.
解答 解:A、无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,硫酸显酸性,在滤纸上滴加硫酸,不变色,故选项正确.
B、紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,稀盐酸显酸性,在滤纸上滴加石蕊溶液,变红色,故选项错误.
C、澄清石灰水能与盐酸反应生成氯化钙和水,但当石灰水过量时,石灰水显碱性,能使酚酞溶液变红色,故选项错误.
D、KOH溶液能与盐酸反应生成氯化钾和水,但当KOH溶液过量时,KOH溶液显碱性,能使酚酞溶液变红色,故选项错误.
故选:A.
点评 本题难度不大,掌握酸的化学性质、常见酸碱指示剂的性质是正确解答本题的关键.

练习册系列答案
相关题目
11.酸碱反应与人们的日常生活和生产有密切的关系.
(1)由于人的胃里有HCl(填化学式),因此胃液分泌过多会引起胃病,服用含有氢氧化铝的药物可缓解病痛的原理是(用化学方程式表示)3HCl+Al(OH)3=AlCl3+3H2O.
(2)人被昆虫叮咬后皮肤红肿起泡,这是由于昆虫在皮肤内注入了少量甲酸(一种酸性物质)所致.把少许下表所列的生活常用品AC(填编号)涂在被咬的皮肤上,痛痒会消失.
(1)由于人的胃里有HCl(填化学式),因此胃液分泌过多会引起胃病,服用含有氢氧化铝的药物可缓解病痛的原理是(用化学方程式表示)3HCl+Al(OH)3=AlCl3+3H2O.
(2)人被昆虫叮咬后皮肤红肿起泡,这是由于昆虫在皮肤内注入了少量甲酸(一种酸性物质)所致.把少许下表所列的生活常用品AC(填编号)涂在被咬的皮肤上,痛痒会消失.
| 物质 | A | B | C | D |
| 肥皂水 | 食醋 | 牙膏 | 食盐水 | |
| pH | 10 | 3 | 9 | 7 |
18. 请根据表中物质回答下列有关问题.
请根据表中物质回答下列有关问题.
(1)上表中的物质属于碱的是Ca(OH)2(用化学式表示).
(2)选用表中的物质作为反应物,写出制取氢氧化钠的化学方程式:
Ca(OH)2+Na2CO3=2NaOH+CaCO3↓;该反应属于复分解反应(填基本反应类型).
(3)某澄清溶液由HNO3、Na2SO4、K2CO3、CuCl2四种物质中的两种组成,向溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量(m)与加入Ba(OH)2溶液的体积(V)的关系如图所示.则该溶液所含的溶质是HNO3、CuCl2;滴加Ba(OH)2后最终反应产生的沉淀是Cu(OH)2..
 请根据表中物质回答下列有关问题.
请根据表中物质回答下列有关问题.| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 生石灰 | 熟石灰 | 纯碱 |
(2)选用表中的物质作为反应物,写出制取氢氧化钠的化学方程式:
Ca(OH)2+Na2CO3=2NaOH+CaCO3↓;该反应属于复分解反应(填基本反应类型).
(3)某澄清溶液由HNO3、Na2SO4、K2CO3、CuCl2四种物质中的两种组成,向溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量(m)与加入Ba(OH)2溶液的体积(V)的关系如图所示.则该溶液所含的溶质是HNO3、CuCl2;滴加Ba(OH)2后最终反应产生的沉淀是Cu(OH)2..
8.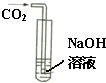 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳气体通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究:
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳气体通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究:
探究一:二氧化碳与氢氧化钠是否发生了反应?
同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡冒出,证明二氧化碳与氢氧化钠发生了反应.
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】
佳佳认为:溶质是Na2CO3
贝贝认为:溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性.
【实验验证】
贝贝为了验证自己的猜想,进行如下实验,请你补充完整
【分析交流】
(1)贝贝滴加过量CaCl2溶液的目的是把碳酸钠充分反应
(2)贝贝过滤后的滤液中的溶质是氢氧化钠
【实验反思】
同学们联想到氢氧化钠溶液与稀硫酸发生中和反应时也观察不到明显现象,为了验证反应确实发生了,有同学设计了如下实验方案:先用pH试纸测定NaOH 溶液的pH,再向其中滴加稀硫酸,边滴边测定混合溶液的pH,当测得pH小于或等于7时,便可证明反应发生了.
请你分析上述方案中,为什么要“当测得pH小于或等于7时”,才能证明反应发生了,原因是排除因硫酸的加入,稀释氢氧化钠溶液而引起pH减小因素的干扰.
 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳气体通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究:
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳气体通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究:探究一:二氧化碳与氢氧化钠是否发生了反应?
同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡冒出,证明二氧化碳与氢氧化钠发生了反应.
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】
佳佳认为:溶质是Na2CO3
贝贝认为:溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性.
【实验验证】
贝贝为了验证自己的猜想,进行如下实验,请你补充完整
| 实验操作 | 实验现象 | 结论 |
| ①取一定量大试管中的溶液于试管中,滴加过量CaCl2溶液,过滤. ②向滤液中滴加酚酞 | 溶液变成红色 | 贝贝的猜想成立 |
(1)贝贝滴加过量CaCl2溶液的目的是把碳酸钠充分反应
(2)贝贝过滤后的滤液中的溶质是氢氧化钠
【实验反思】
同学们联想到氢氧化钠溶液与稀硫酸发生中和反应时也观察不到明显现象,为了验证反应确实发生了,有同学设计了如下实验方案:先用pH试纸测定NaOH 溶液的pH,再向其中滴加稀硫酸,边滴边测定混合溶液的pH,当测得pH小于或等于7时,便可证明反应发生了.
请你分析上述方案中,为什么要“当测得pH小于或等于7时”,才能证明反应发生了,原因是排除因硫酸的加入,稀释氢氧化钠溶液而引起pH减小因素的干扰.
15.在下列各反应中,属于复分解反应的是( )
| A. | H2SO4+Zn═ZnSO4+H2↑ | B. | C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2↑ | ||
| C. | 2O2+CH4$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | D. | H2SO4+Cu(OH)2═Cu SO4+2H2O |
12.如图是元素周期表中的一种元素,下列有关该元素的信息正确的是( )


| A. | 原子序数是12 | B. | 它是非金属元素 | ||
| C. | 核内质子数是24.31 | D. | 相对原子质量是12 |
