题目内容
7.钢铁是日常生产、生活中最常见的金属,请完成与其有关的试题.(1)铁在潮湿的空气中表面易生成一种暗红色的固体,其主要成分的化学式为O3.
(2)铁丝在纯净的氧气中燃烧的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 .
(3)将一定量的铁粉加入到足量的硫酸中,反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
(4)铁丝与硫酸铜溶液的反应现象为铁丝表面有红色物质生成,溶液由蓝色逐渐变成浅绿色,方程式为Fe+CuSO4=FeSO4+Cu.
分析 (1)根据铁锈的主要成分为三氧化二铁分析回答;
(2)根据铁在氧气中燃烧生成了四氧化三铁进行分析回答.
(3)根据铁能与硫酸反应分析回答;
(4)根据铁能与硫酸铜溶液的反应分析回答.
解答 解:(1)铁在潮湿的空气中与水和氧气共同作用而生锈,主要成分是三氧化二铁,可用化学式Fe2O3表示;
(2)细铁丝在纯氧中燃烧生成四氧化三铁,反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 ;
(3)将一定量的铁粉加入到足量的硫酸中,铁与硫酸反应生成了硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑.
(4)铁排在铜的前面,故铁可以把硫酸铜中的铜置换出来,铁丝与硫酸铜溶液的反应现象为:铁丝表面有红色物质生成,溶液由蓝色逐渐变成浅绿色,方程式为Fe+CuSO4=FeSO4+Cu.
故答案为:(1)Fe2O3;(2)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;(3)Fe+H2SO4=FeSO4+H2↑.(4)铁丝表面有红色物质生成,溶液由蓝色逐渐变成浅绿色Fe+CuSO4=FeSO4+Cu.
点评 本题考查了化学式和化学方程式的书写,掌握金属活动性顺序表的应用是解答本题的基础.

练习册系列答案
相关题目
18.化学实验中常用到木条.下列实验中木条的使用不能达到目的是( )
| A. | 将带火星的木条伸入集气瓶内,检验瓶内气体是否为氧气 | |
| B. | 将燃着的木条放在集气瓶口,检验氢气是否集满 | |
| C. | 分别在酒精灯上加热木条和石子,证明燃烧需要可燃物 | |
| D. | 将木条平放在蜡烛火焰中,比较各层火焰温度的高低 |
2.水是生命之源,下列关于水的说法正确的是( )
| A. | 澄清的矿泉水是纯水 | B. | 肥皂水可鉴别硬水和软水 | ||
| C. | 过滤可以除去水中所有的杂质 | D. | 填埋垃圾不会导致水体污染 |
12.下列含氯物质中,氯元素化合价最低的是( )
| A. | Ca(ClO)2 | B. | Cl2 | C. | NH4Cl | D. | KClO3 |


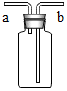 如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题:
如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题:
