题目内容
7. (1)为延长食品保质期,常在食品中添加苯甲酸(C6H5COOH)作为防腐剂.回答下列问题:
(1)为延长食品保质期,常在食品中添加苯甲酸(C6H5COOH)作为防腐剂.回答下列问题:①苯甲酸是由三种元素组成;②苯甲酸中碳元素与氢元素的质量比为14:1(最简整数比).
(2)小明称取黄铜(铜锌合金)样品10.0克,再用100.0克
稀硫酸溶液逐滴滴入,测得实验数据如图所示.求:
①该铜锌合金中,铜和锌的质量比是7:13(最简整数比).
②所用稀硫酸溶液中溶质的质量分数是多少?
分析 (1)根据苯甲酸的化学式来分析其元素组成;利用化学式和相对原子质量来计算三种元素的质量比;
(2)根据质量守恒分析完全反应生成H2的质量,结合方程式可以求解锌的质量和硫酸的质量,在进一步求解;
解答 解:(1)由化学式C6H5COOH可知苯甲酸是由C、H、O三种元素组成;其中C、H种元素的质量比为(12×7):(1×6)=14:1;故填:三;14:1;
(2)①完全反应生成H2的质量为10.0g+50g-59.8g=0.2g
设50g稀硫酸中H2SO4的质量为x,锌的质量为y.
Zn+H2SO4=ZnSO4+H2↑
65 98 2
y x 0.2g
$\frac{65}{y}=\frac{98}{x}=\frac{2}{0.2g}$
x=9.8g,y=6.5g
该铜锌合金中,铜和锌的质量比是(10.0g-6.5g):6.5g=7:13;故填:7:13;
②稀硫酸中溶质的质量分数为$\frac{9.8g}{50g}$×100%=19.6%
答:稀硫酸中溶质的质量分数为19.6%.
点评 本题主要考查学生运用化学式和化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.

练习册系列答案
相关题目
18.关于酸雨的下列说法正确的是( )
| A. | pH>7的降雨称为酸雨 | B. | pH<7的降雨称为酸雨 | ||
| C. | pH>5.6的降雨称为酸雨 | D. | pH<5.6的降雨称为酸雨 |
2. 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如右图所示.下列说法正确的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如右图所示.下列说法正确的是( )
 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如右图所示.下列说法正确的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如右图所示.下列说法正确的是( )| A. | 该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中 | |
| B. | 图中b点表示硫酸和氢氧化钠溶液恰好完全反应 | |
| C. | 图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4 | |
| D. | 向c点溶液中滴入紫色石蕊试液,溶液变蓝色 |
12.下列区分物质的试剂或方法错误的是( )
| A. | 用闻气味的方法区分酒精和食醋 | B. | 用肥皂水鉴别硬水和软水 | ||
| C. | 用水区分硝酸铵和生石灰 | D. | 用手感法鉴别腈纶和羊毛 |
14.比较推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 镁条可在空气中燃烧,故铁丝也可在空气中燃烧 | |
| B. | 金刚石很硬,故石墨也很硬 | |
| C. | 氢氧化铝可治疗胃酸过多,故氢氧化钠也可用于治疗胃酸过多症 | |
| D. | 生铁比纯铁硬,故黄铜比纯铜硬 |
 A、B、C、D的物质类别各不相同,C是胃酸的主要成分,A是一种红棕色固体,D含有四种元素.它们之间的反应或转化关系如图所示(部分物质和反应条件已略去),请写出下列反应的化学反应方程式:
A、B、C、D的物质类别各不相同,C是胃酸的主要成分,A是一种红棕色固体,D含有四种元素.它们之间的反应或转化关系如图所示(部分物质和反应条件已略去),请写出下列反应的化学反应方程式:



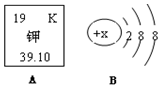 钾在人体内起着调节体液平衡的作用,如图A是钾元素在元素周期表中的相关信息.
钾在人体内起着调节体液平衡的作用,如图A是钾元素在元素周期表中的相关信息.