题目内容
将有机物R和氧气置于一个完全封闭的容器中引燃,测得反应前后各物质的质量如下表.
| 物质 | R | 氧气 | 二氧化碳 | 水 |
| 反应前质量/g | 2.3 | 10.0 | 0 | 0 |
| 反应后质量/g | X | 5.2 | 4.4 | Y |
下列说法正确的是
- A.X的值为0
- B.R的化学式为C2H6
- C.该反应中CO2与H2O的化学计量数之比为2:3
- D.该反应属于分解反应
AC
分析:因为氧气剩余,所以R的量不足,X=0;根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,可计算Y的值;先计算出二氧化碳和水中的氧元素的质量,与消耗的氧气的质量比较,推测R中是否含有氧元素;根据二氧化碳和水的质量,可推测其化学计量数;因为反应物为R和氧气,所以不是分解反应.
解答:A、因为氧气未耗尽,所以R的量不足,X=0,故A正确;
B、因为反应物R为2.3克,生成二氧化碳4.4,则可知二氧化碳中的碳元素的质量为4.4×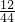 ×100%=1.2克,根据质量守恒定律,反应物R中的碳元素质量=1.2克,C%=
×100%=1.2克,根据质量守恒定律,反应物R中的碳元素质量=1.2克,C%= ,而C2H6中C%=
,而C2H6中C%= ,故B不符合;
,故B不符合;
C、因为反应物R为2.3克和氧气10-5.2=4.8克,根据质量守恒定律可知,生成二氧化碳4.4,所以生成的水为2.7克,设CO2与H2O的化学计量数分别为x,y, ,x:y=2:3,故C正确;
,x:y=2:3,故C正确;
D、因为反应物为R和氧气,所以不是分解反应,故D错误.
故选A、C.
点评:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和;掌握反应类型的判定.
分析:因为氧气剩余,所以R的量不足,X=0;根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,可计算Y的值;先计算出二氧化碳和水中的氧元素的质量,与消耗的氧气的质量比较,推测R中是否含有氧元素;根据二氧化碳和水的质量,可推测其化学计量数;因为反应物为R和氧气,所以不是分解反应.
解答:A、因为氧气未耗尽,所以R的量不足,X=0,故A正确;
B、因为反应物R为2.3克,生成二氧化碳4.4,则可知二氧化碳中的碳元素的质量为4.4×
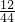 ×100%=1.2克,根据质量守恒定律,反应物R中的碳元素质量=1.2克,C%=
×100%=1.2克,根据质量守恒定律,反应物R中的碳元素质量=1.2克,C%= ,而C2H6中C%=
,而C2H6中C%= ,故B不符合;
,故B不符合;C、因为反应物R为2.3克和氧气10-5.2=4.8克,根据质量守恒定律可知,生成二氧化碳4.4,所以生成的水为2.7克,设CO2与H2O的化学计量数分别为x,y,
 ,x:y=2:3,故C正确;
,x:y=2:3,故C正确;D、因为反应物为R和氧气,所以不是分解反应,故D错误.
故选A、C.
点评:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和;掌握反应类型的判定.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
将有机物R和氧气置于一个完全封闭的容器中引燃,测得反应前后各物质的质量如下表.
下列说法正确的是( )
| 物质 | R | 氧气 | 二氧化碳 | 水 |
| 反应前质量/g | 2.3 | 10.0 | 0 | 0 |
| 反应后质量/g | X | 5.2 | 4.4 | Y |
| A、X的值为0 |
| B、R的化学式为C2H6 |
| C、该反应中CO2与H2O的化学计量数之比为2:3 |
| D、该反应属于分解反应 |
将有机物R和氧气置于一个完全封闭的容器中引燃,测得反应前后各物质的质量如下表。
|
物质 |
R |
氧气 |
二氧化碳 |
水 |
|
反应前质量/ g |
2.3 |
10.0 |
0 |
0 |
|
反应后质量/ g |
0 |
5.2 |
4.4 |
Y |
下列说法正确的是 ( )
A.Y的值为3.1
B.R的化学式为C2H6
C.该反应中CO2与H2O的化学计量数之比为2∶3
D.该反应属于分解反应
将有机物R和氧气置于一个完全封闭的容器中引燃,测得反应前后各物质的质量如下表。
|
物质 |
R |
氧气 |
二氧化碳 |
水 |
|
反应前质量/ g |
2.3 |
10.0 |
0 |
0 |
|
反应后质量/ g |
0 |
5.2 |
4.4 |
Y |
下列说法正确的是
A.Y的值为3.1
B.R的化学式为C2H6
C.该反应中CO2与H2O的化学计量数之比为2∶3
D.该反应属于分解反应
将有机物R和氧气置于一个完全封闭的容器中引燃,测得反应前后各物质的质量如下表.
下列说法正确的是( )
A.X的值为0
B.R的化学式为C2H6
C.该反应中CO2与H2O的化学计量数之比为2:3
D.该反应属于分解反应
| 物质 | R | 氧气 | 二氧化碳 | 水 |
| 反应前质量/g | 2.3 | 10.0 | ||
| 反应后质量/g | X | 5.2 | 4.4 | Y |
A.X的值为0
B.R的化学式为C2H6
C.该反应中CO2与H2O的化学计量数之比为2:3
D.该反应属于分解反应