题目内容
中各和反应是酸碱盐之间的一类重要反应,也是复分解反应中的一个特殊类型,盐酸和氢氧化钠溶液的反应是中和反应的典型代表,下图是有关此反应发生过程中各项的变化如下图,请分析:
(1)根据图四pH变化图象判断,该反应的实验过程是按照图二中的图 (填“甲”或“乙”)进行;
(2)当图一中的溶液恰好变成无色的时候,是图四中A、B、C 三点中的点 (填“A”、“B”或“C”,下同),是图四中的点 时的溶液;加入紫色石蕊试液会呈现红色的是图四中的点 时的溶液,此时溶液中一定含有的阳离子有 ;

(3)为了证明盐酸与氢氧化钠溶液反应的生成物,小明的探究过程如下:
实验过程:向装有一定量稀盐酸的试管中滴加氢氧化钠溶液,振荡后再滴加硝酸银溶液.
观察现象:出现白色沉淀.
得出结论:证明生成了氯化钠.
小思认为该结论不正确.合理解释是 .
(1)根据图四pH变化图象判断,该反应的实验过程是按照图二中的图
(2)当图一中的溶液恰好变成无色的时候,是图四中A、B、C 三点中的点

(3)为了证明盐酸与氢氧化钠溶液反应的生成物,小明的探究过程如下:
实验过程:向装有一定量稀盐酸的试管中滴加氢氧化钠溶液,振荡后再滴加硝酸银溶液.
观察现象:出现白色沉淀.
得出结论:证明生成了氯化钠.
小思认为该结论不正确.合理解释是
考点:中和反应及其应用,溶液的酸碱性与pH值的关系,盐的化学性质
专题:常见的酸 酸的通性
分析:(1)该图象中溶液的起始pH值大于7,所以是将盐酸滴加到氢氧化钠溶液中,曲线上B点的pH=7,说明此时盐酸和氢氧化钠溶液恰好完全反应;
(2)氢氧化钠溶液和盐酸可以发生中和反应生成氯化钠和水,恰好完全反应时其PH等于7,氢氧化钠过量时显碱性,盐酸过量时显酸性.据此分析解答;
(3)氯离子能与银离子结合成白色沉淀.
(2)氢氧化钠溶液和盐酸可以发生中和反应生成氯化钠和水,恰好完全反应时其PH等于7,氢氧化钠过量时显碱性,盐酸过量时显酸性.据此分析解答;
(3)氯离子能与银离子结合成白色沉淀.
解答:解:
(1)该图象中溶液的起始pH值大于7,所以是将盐酸滴加到氢氧化钠溶液中,该实验操作是按照图乙进行的;
(2)曲线上B点的pH=7,说明此时盐酸和氢氧化钠溶液恰好完全反应,溶液由碱性变为中性,碱性溶液能使酚酞试液变红,中性溶液不能使其变色,故此时溶液由红色变为无色;由图象可知C点溶液pH小于7呈酸性,加入紫色石蕊试液会呈现红色,所以此时盐酸过量,同时由于两者反应会生成氯化钠,所以溶液中含有氯化氢和氯化钠两种溶质,此时溶液中一定含有的阳离子有Na+和H+;
(3)不但氯化钠溶液能与硝酸银溶液反应产生氯化银白色沉淀,盐酸也能与硝酸银溶液反应产生氯化银白色沉淀,故填:稀盐酸也会与硝酸银反应生成白色的氯化银沉淀.
答案:
(1)乙
(2)B B C Na+和H+
(3)稀盐酸也会与硝酸银反应生成白色的氯化银沉淀.
(1)该图象中溶液的起始pH值大于7,所以是将盐酸滴加到氢氧化钠溶液中,该实验操作是按照图乙进行的;
(2)曲线上B点的pH=7,说明此时盐酸和氢氧化钠溶液恰好完全反应,溶液由碱性变为中性,碱性溶液能使酚酞试液变红,中性溶液不能使其变色,故此时溶液由红色变为无色;由图象可知C点溶液pH小于7呈酸性,加入紫色石蕊试液会呈现红色,所以此时盐酸过量,同时由于两者反应会生成氯化钠,所以溶液中含有氯化氢和氯化钠两种溶质,此时溶液中一定含有的阳离子有Na+和H+;
(3)不但氯化钠溶液能与硝酸银溶液反应产生氯化银白色沉淀,盐酸也能与硝酸银溶液反应产生氯化银白色沉淀,故填:稀盐酸也会与硝酸银反应生成白色的氯化银沉淀.
答案:
(1)乙
(2)B B C Na+和H+
(3)稀盐酸也会与硝酸银反应生成白色的氯化银沉淀.
点评:本题综合考查了盐酸和氢氧化钠发生反应的实质、现象等相关知识,通过图象反映了二者反应的进行情况,能较好考查学生对所学知识的应用和解决问题的能力.

练习册系列答案
相关题目
掌握化学用语是学好化学的关键,下列化学用语与含义相符的是( )
| A、P2O5-五氧化二磷 |
| B、2H-2个氢元素 |
| C、O2-2个氧原子 |
| D、Na-钠离子 |
下列四个图象中,能正确反映对应变化关系的是( )
A、 向一定量的稀盐酸中加入氧化铁 向一定量的稀盐酸中加入氧化铁 |
B、 向一定量的氢氧化钠溶液中滴加稀盐酸 向一定量的氢氧化钠溶液中滴加稀盐酸 |
C、 向一定量的硫酸铜溶液中加入铁粉 向一定量的硫酸铜溶液中加入铁粉 |
D、 向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳 向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳 |

 体育中考时很多同学从药店购买葡萄糖注射液,想在长跑前给自己补充能量和体液.为测定葡萄糖注射液的溶质质量分数与标签所示是否相符(见图),化学兴趣小组的同学采用了如下方法:取50g该注射液于烧杯中,逐滴滴加新制的氢氧化铜并加热,至不再产生沉淀为止,经过滤、洗涤、干燥后,称量固体质量为2.0g.该反应原理为:C6H12O6+2Cu(OH)2
体育中考时很多同学从药店购买葡萄糖注射液,想在长跑前给自己补充能量和体液.为测定葡萄糖注射液的溶质质量分数与标签所示是否相符(见图),化学兴趣小组的同学采用了如下方法:取50g该注射液于烧杯中,逐滴滴加新制的氢氧化铜并加热,至不再产生沉淀为止,经过滤、洗涤、干燥后,称量固体质量为2.0g.该反应原理为:C6H12O6+2Cu(OH)2
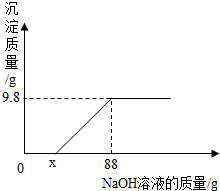 在绵阳市2014实验操作考试结束后,同学们在帮助老师整理实验室时,对酸性硫酸铜溶液(含有硫酸)产生了兴趣,在经老师允许后他们经行了如下的探究,取一定量的酸性硫酸铜溶液,向混合溶液中逐滴加入10%的氢氧化钠溶液,记录了如图所示的曲线关系.请根据曲线关系完成以下问题:
在绵阳市2014实验操作考试结束后,同学们在帮助老师整理实验室时,对酸性硫酸铜溶液(含有硫酸)产生了兴趣,在经老师允许后他们经行了如下的探究,取一定量的酸性硫酸铜溶液,向混合溶液中逐滴加入10%的氢氧化钠溶液,记录了如图所示的曲线关系.请根据曲线关系完成以下问题: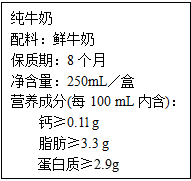 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体(Ca5(PO4)3(OH))形式存在,其相对分子质量为502.牛奶含钙丰富又易被吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签的部分说明.请仔细阅读后回答下列问题:
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体(Ca5(PO4)3(OH))形式存在,其相对分子质量为502.牛奶含钙丰富又易被吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签的部分说明.请仔细阅读后回答下列问题: