题目内容
元素周期表是学习和研究化学的重要工具,它的内容十分丰富.试回答: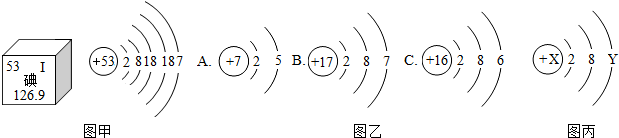
(1)碘原子的结构示意图如甲所示,则它位于元素周期表中的第 周期,中子数为 ,该元素的化学性质与图乙中 (选填A、B、C) 的化学性质相似.
(2)某原子的结构示意图如图丙,已知该粒子在化学反应中易得到2个电子形成稳定结构,X= ,该元素得到两个电子后形成的离子符号是 .

(1)碘原子的结构示意图如甲所示,则它位于元素周期表中的第
(2)某原子的结构示意图如图丙,已知该粒子在化学反应中易得到2个电子形成稳定结构,X=
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图,化学符号及其周围数字的意义
专题:化学用语和质量守恒定律
分析:(1)根据元素周期数等于核外电子层数,相对原子质量≈质子数+中子数、最外层电子数决定元素的化学性质来分析;
(2)根据题意,当质子数=核外电子数,为原子,该粒子在化学反应中易得到2个电子形成稳定结构,据此进行分析解答.
(2)根据题意,当质子数=核外电子数,为原子,该粒子在化学反应中易得到2个电子形成稳定结构,据此进行分析解答.
解答:解:(1)碘原子核外有5个电子层,故位于第五周期;中子数=相对原子质量-质子数=127-53=74;碘原子最外层有7个电子,与B化学性质类似;故填:五;74;B;(2)该粒子在化学反应中易得到2个电子形成稳定结构,则该原子的最外层电子数为6,即Y=6;当质子数=核外电子数,为原子,则X=2+8+6=16;核内质子数为16,
写出的离子为硫离子,其离子符号为:S2-.故答案为:16;S2-.
写出的离子为硫离子,其离子符号为:S2-.故答案为:16;S2-.
点评:本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.灵活运用元素周期表中元素的信息是正确解题的关键.

练习册系列答案
相关题目
T℃时将少量生石灰加到一定质量的饱和澄清石灰水中,溶液的温度升高,再将其恢复到T℃(不考虑水的蒸发),下列四位同学对变化后溶液的分析错误的是( )
| A、溶质的质量分数与原溶液的相同 |
| B、溶剂的质量比原溶液的减少了 |
| C、溶质的质量与原溶液的相同 |
| D、析出固体后的溶液是不饱和溶液 |
下列有关分子、原子和离子的说法正确的是( )
| A、分子是化学变化中的最小的粒子 |
| B、原子是保持化学性质的最小粒子 |
| C、分子、原子、离子都可以直接构成物质 |
| D、在化学反应中,任何离子都不能再分 |
下列对课本中相关实验的分析不正确的是( )
| A、电解水实验能说明水有氢、氧两种元素组成 |
| B、黄豆与芝麻混合的实验能说明分子之间有空隙 |
| C、氢氧化钠与硫酸铜溶液反应前后质量的测定实验能说明化学变化遵循质量守恒定律 |
| D、二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气 |
下列各组物质按照单质、酸、碱的顺序排列的是( )
| A、氮气 盐酸 乙醇 |
| B、石墨 干冰 纯碱 |
| C、水银 冰醋酸 苛性钠 |
| D、冰 硫酸 熟石灰 |
 某校化学实验兴趣小组想了解水的组成,他们做了如下实验:
某校化学实验兴趣小组想了解水的组成,他们做了如下实验: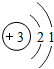 ,易失去最外层一个电子,锂离子的符号是
,易失去最外层一个电子,锂离子的符号是