题目内容
Na2SO4和Na2CO3的混合物12.4g与100g稀硫酸恰好完全反应,产生2.20g气体.求:
(1)原混合物中Na2SO4的质量分数;
(2)反应后所得溶液中溶质的质量分数(结果保留到0.1).
(1)原混合物中Na2SO4的质量分数;
(2)反应后所得溶液中溶质的质量分数(结果保留到0.1).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据碳酸钠与硫酸反应的化学方程式,由生成气体二氧化碳的质量计算混合物中碳酸钠质量,即可解决原混合物中Na2SO4的质量分数;
(2)恰好完全反应后所得溶液为硫酸钠溶液,其中溶质硫酸钠由混合物中硫酸钠与反应生成硫酸钠的质量和,再利用质量守恒定律求得反应后溶液质量,即可计算出反应后溶液中Na2SO4的质量分数.
(2)恰好完全反应后所得溶液为硫酸钠溶液,其中溶质硫酸钠由混合物中硫酸钠与反应生成硫酸钠的质量和,再利用质量守恒定律求得反应后溶液质量,即可计算出反应后溶液中Na2SO4的质量分数.
解答:解:设原混合物中Na2CO3的质量为x,生成Na2SO4质量为y
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
106 142 44
x y 2.20g
=
,
=
x=5.30g,y=7.10g
(1)原混合物中硫酸钠的质量分数:
×100%=57.3%
(2)溶液中硫酸钠的质量分数:
×100%=12.9%
答:(1)原混合物中Na2SO4的质量分数为57.3%;
(2)反应后溶液中Na2SO4的质量分数为12.9%.
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
106 142 44
x y 2.20g
| 106 |
| x |
| 44 |
| 2.20g |
| 142 |
| y |
| 44 |
| 2.20g |
x=5.30g,y=7.10g
(1)原混合物中硫酸钠的质量分数:
| 12.4g-5.30g |
| 12.4g |
(2)溶液中硫酸钠的质量分数:
| 12.4g-5.30g+7.10g |
| 12.4g+100g-2.20g |
答:(1)原混合物中Na2SO4的质量分数为57.3%;
(2)反应后溶液中Na2SO4的质量分数为12.9%.
点评:根据质量守恒定律,恰好完全反应后的硫酸钠溶液质量=原混合物的质量+所加入稀硫酸的质量-反应放出气体二氧化碳的质量.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
水的下列性质中,属于化学性质的是( )
| A、无色 |
| B、水通电后分解为氢气和氧气 |
| C、受热后成为水蒸气 |
| D、常温下为液体 |
 某化肥包装上的标签如图所示.
某化肥包装上的标签如图所示.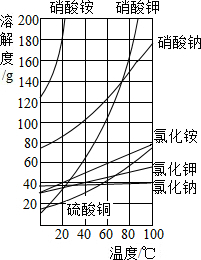 一些物质的溶解度曲线如图,回答下列问题.
一些物质的溶解度曲线如图,回答下列问题.