题目内容
过氧化氢(H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.(1)实验室如果采用分解过氧化氢来制取氧气,还需加入 作 ,它的作用是 .
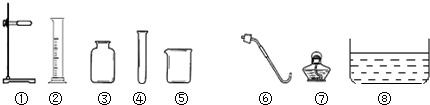
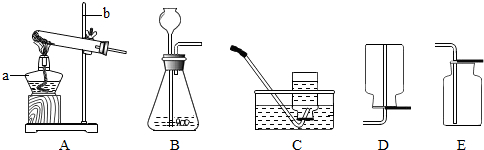
(2)现有下列仪器,请选择一组仪器,使它既能制取氧气,又能制取二氧化碳.

所选择仪器的序号有 .如选择C仪器,实验过程中的优点是 ;
制取氧气时,MnO2装在 ;制取二氧化碳时液体药品装在 ,
用该装置制取二氧化碳的化学反应式为 .
【答案】分析:(1)根据实验室用过氧化氢制取氧气的反应原理及催化剂的作用进行分析解答即可;
(2)根据制取二氧化碳和氧气共同装置的特点是固液常温型的发生装置和向上排空气法收集的装置选择仪器;分液漏斗的作用可以控制液体的流速;固体放在锥形瓶内,液体放在分液漏斗内;实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的方程式.
解答:解:(1)用过氧化氢制取氧气时,常加入二氧化锰,二氧化锰在此反应中作催化剂,起催化作用,能加快过氧化氢分解产生氧气的速率;
(2)制取二氧化碳和氧气共同装置的特点是固液常温型的发生装置,需要的仪器有:ACE或ADE;用向上排空气法收集的装置的装置有G;分液漏斗的作用可以控制液体的流速,从而控制反应的速率;制取氧气时,MnO2装在锥形瓶内;制取二氧化碳时液体药品稀盐酸装在分液漏斗内;稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;
故答案为:(1)二氧化锰;催化剂;起催化作用,能加快过氧化氢分解产生氧气的速率;(2)ADEG或ACEG;可以控制反应的速率;锥形瓶内;分液漏斗内;CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评:本题考查了常见气体仪器和二氧化碳的制取装置、收集方法等需要仪器的选择及催化剂的作用,关键是明确发生装置、收集方法选择的依据及催化剂的定义.
(2)根据制取二氧化碳和氧气共同装置的特点是固液常温型的发生装置和向上排空气法收集的装置选择仪器;分液漏斗的作用可以控制液体的流速;固体放在锥形瓶内,液体放在分液漏斗内;实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的方程式.
解答:解:(1)用过氧化氢制取氧气时,常加入二氧化锰,二氧化锰在此反应中作催化剂,起催化作用,能加快过氧化氢分解产生氧气的速率;
(2)制取二氧化碳和氧气共同装置的特点是固液常温型的发生装置,需要的仪器有:ACE或ADE;用向上排空气法收集的装置的装置有G;分液漏斗的作用可以控制液体的流速,从而控制反应的速率;制取氧气时,MnO2装在锥形瓶内;制取二氧化碳时液体药品稀盐酸装在分液漏斗内;稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;
故答案为:(1)二氧化锰;催化剂;起催化作用,能加快过氧化氢分解产生氧气的速率;(2)ADEG或ACEG;可以控制反应的速率;锥形瓶内;分液漏斗内;CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评:本题考查了常见气体仪器和二氧化碳的制取装置、收集方法等需要仪器的选择及催化剂的作用,关键是明确发生装置、收集方法选择的依据及催化剂的定义.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
 实验室中常用高锰酸钾受热分解制取氧气.
实验室中常用高锰酸钾受热分解制取氧气.