题目内容
1.化学方程式的书写是学好化学的关键,但是很多同学在刚刚学习化学方程式书写时常常会犯一些错误,具体概括如下:①生成物化学式书写错误 ②未配平 ③遗漏反应条件 ④“↑”或“↓”使用不当
请你判断下列化学方程式的错误类型(填序号).
| 序号 | 化学方程式 | 错误类型 |
| (1) | 镁条燃烧:Mg+O2$\frac{\underline{\;点燃\;}}{\;}$ MgO2 | ① |
| (2) | 用硫酸铜溶液和氢氧化钠溶液混合: CuSO4+NaOH═Na2SO4+Cu(OH)2↓ | ② |
| (3) | 高炉冶炼赤铁矿:3CO+Fe2O3═Fe+3CO2↑ | ③④ |
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
解答 解:(1)生成物氧化镁化学式错误,正确的化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$ 2MgO,故选①;
(2)化学方程式未配平,正确的化学方程式为:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓;故选②;
(3)化学方程式缺少反应的条件,当反应物中有气体,生成物中的气体不能标气体符号,
故正确的化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Fe+3CO2;故选③④;
故答案为:(1)①(2)②(3)③④
点评 本题难度不大,考查学生根据反应原理书写化;学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 同步奥数系列答案
同步奥数系列答案
相关题目
5.以下有关水的说法,错误的是( )
| A. | 水能无限溶解任何物质且溶解时都不会吸热或放热 | |
| B. | 生命活动离不开水 | |
| C. | 净化水的方法有吸附、沉淀、过滤和蒸馏等 | |
| D. | 用肥皂水可以检验硬水和软水 |
12.取一定质量的CaCO3高温加热一段时间后,冷却,测得剩余固体的质量为10.6g,剩余固体中碳元素的质量为0.6g,下列判断正确的是( )
| A. | 生成了2.2g CO2 | B. | 剩余CaCO3的质量为10.0g | ||
| C. | 生成了10.6g CaO | D. | 原来CaCO3的质量为15.0g |
10.将一定量的稀HCl加入到盛有NaOH溶液的烧杯中,未观察到明显现象.对“反应后溶液中的溶质是什么?”同学们提出了以下的猜想:
猜想一:只有NaCl; 猜想二:有NaCl和HCl; 猜想三:有NaCl和NaOH
为探究溶质的成分,他们进行以下实验:
(1)取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,则溶液中一定没有的成分是NaOH(或氢氧化钠).
(2)他们选用了pH试纸、AgNO3溶液、Na2CO3溶液,继续进行下面的实验:
根据上述实验结果,同学们得出猜想二是正确.
(3)评价反思:甲同学反思发现在上表中的实验操作,存在一处明显错误,将pH试纸浸入溶液中;乙同学对上表中的某一实验所得出结论也有异议,理由NaC1与AgNO3反应也会生成白色沉淀,不能证明一定有HCl存在.
猜想一:只有NaCl; 猜想二:有NaCl和HCl; 猜想三:有NaCl和NaOH
为探究溶质的成分,他们进行以下实验:
(1)取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,则溶液中一定没有的成分是NaOH(或氢氧化钠).
(2)他们选用了pH试纸、AgNO3溶液、Na2CO3溶液,继续进行下面的实验:
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加AgNO3溶液 |
| 实验操作 | 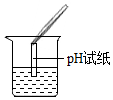 | 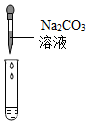 |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
(3)评价反思:甲同学反思发现在上表中的实验操作,存在一处明显错误,将pH试纸浸入溶液中;乙同学对上表中的某一实验所得出结论也有异议,理由NaC1与AgNO3反应也会生成白色沉淀,不能证明一定有HCl存在.
11.对下列现象的解释或结论错误的是( )
| 选项 | 现象 | 解释或结论 |
| A | 花香四溢 | 分子不断运动 |
| B | 稀盐酸、稀硫酸都能使石蕊变红色 | 稀盐酸、稀硫酸中都含有大量的H+ |
| C | 绿色植物的光合作用吸收二氧化碳 | 这是自然界中碳循环中的重要一环 |
| D | 把燃着的木条伸入集气瓶中,木条熄灭 | 瓶中的气体是二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
 化学用语是九年级化学的重要学习内容之一,也是学好化学的关键之一.请根据要求填写相应的化学符号.
化学用语是九年级化学的重要学习内容之一,也是学好化学的关键之一.请根据要求填写相应的化学符号. (1)如图是某趣味实验装置图,挤压胶头滴管后,可观察到气球变大,其是原因用化学方程式表示为:2NaOH+CO2═Na2CO3+H2O.
(1)如图是某趣味实验装置图,挤压胶头滴管后,可观察到气球变大,其是原因用化学方程式表示为:2NaOH+CO2═Na2CO3+H2O.