题目内容
5.已知A、B、C、D、E、F、G、H、I均为初中化学常见的物质.其中E、G为常见金属,E是目前世界上产量最高的金属,G呈紫红色;I是地壳中含量最高的元素所形成的常见气体单质;人体胃液中含有A,可帮助消化.根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出)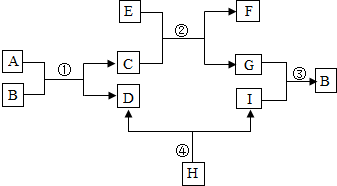
(1)E的名称是铁,B的化学式是CuO. H的化学式是H2O2.
(2)写出反应②的化学方程式:Fe+CuCl2=Cu+FeCl2.写出反应④的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)上图中涉及到D基本反应类型.
A.一种 B.二种 C.三种 D.四种.
分析 根据A、B、C、D、E、F、G、H、I均为初中化学常见的物质,E、G为常见金属,E是目前世界上产量最高的金属,G呈紫红色,所以E是铁,G是铜,I是地壳中含量最高的元素所形成的常见气体单质,所以I是氧气,人体胃液中含有A,可帮助消化,所以A是盐酸,氧气和铜反应会生成氧化铜,所以B是氧化铜,氧化铜和盐酸反应生成氯化铜和水,H会生成氧气和D,所以H是过氧化氢溶液,D是水,C是氯化铜,铁和氯化铜反应生成氯化亚铁和铜,所以F是氯化亚铁,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E、F、G、H、I均为初中化学常见的物质,E、G为常见金属,E是目前世界上产量最高的金属,G呈紫红色,所以E是铁,G是铜,I是地壳中含量最高的元素所形成的常见气体单质,所以I是氧气,人体胃液中含有A,可帮助消化,所以A是盐酸,氧气和铜反应会生成氧化铜,所以B是氧化铜,氧化铜和盐酸反应生成氯化铜和水,H会生成氧气和D,所以H是过氧化氢溶液,D是水,C是氯化铜,铁和氯化铜反应生成氯化亚铁和铜,所以F是氯化亚铁,经过验证,推导正确,所以E是铁,B是CuO,H是H2O2;
(2)反应②是铁和氯化铜反应生成氯化亚铁和铜,化学方程式为:Fe+CuCl2=Cu+FeCl2;
反应④是过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)图中涉及的反应为:①CuO+2HCl=CuCl2+H2O,为复分解反应;
②Fe+CuCl2=FeCl2+Cu,为置换反应;
③2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,为化合反应;
④2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,为分解反应,故选:D.
故答案为:(1)铁,CuO,H2O2;
(2)Fe+CuCl2=Cu+FeCl2;
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)D.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 下表是a、b、c三种物质在不同温度时的溶解度,请根据表中数据回答:
下表是a、b、c三种物质在不同温度时的溶解度,请根据表中数据回答:| 温度/℃ | 0 | 20 | 30 | 40 | 60 | |
| 溶解度/g | 物质a | 13.3 | 31.6 | 45.8 | 63.9 | 110 |
| 物质b | 21.4 | 9.84 | 7.24 | 5.63 | 3.87 | |
| 物质c | 11.9 | 21.7 | 28.4 | 36.6 | 59.2 | |
(2)如图所示,现有20℃时等质量的a、b两物质的饱和溶液,试管底部有等质量的a、b剩余,向烧杯的水中加入氢氧化钠固体,则对相关变化判断正确的有C.(析出的固体中不含水,不考虑溶剂的蒸发)
A.b溶液将由饱和变成不饱和
B.a溶液中溶剂质量等于b溶液中溶剂质量
C.变化后a溶液的溶质质量分数大于b溶液的溶质质量分数.
| A. | 在某固体物质中加入稀盐酸,产生大量气泡$\stackrel{推测}{→}$该物质一定是碳酸盐 | |
| B. | 芝麻和黄豆混合前总体积大于混合后体积$\stackrel{推测}{→}$构成物质的分子之间存在着空隙 | |
| C. | 轻质带电小球A放在另一个轻质小球B旁受力偏转$\stackrel{推测}{→}$B球与A球带异种电荷 | |
| D. | 将干冷的烧杯罩在蜡烛的火焰上方,内壁出现小水珠$\stackrel{推测}{→}$蜡烛中含有氢元素 |
①可能是2.5克氢气和2.5克氧气 ②可能是1克氢气和4克氧气
③可能是0.5克氢气和4.5克氧气 ④可能是0.5克氢气和4克氧气.
| A. | 只有①正确 | B. | 只有②③正确 | C. | ①②③都正确 | D. | 只有④正确 |
| A. |  熄灭酒精灯 | B. |  闻气味 | C. |  制作血涂片 | D. |  滴加试液 |

 如图,一辆载满电石的货车在雨中行驶时突然燃起大火,并伴有大量黑烟.某化学小组对电石中碳化钙(CaC2)的性质产生了兴趣,进行了下列探究活动.
如图,一辆载满电石的货车在雨中行驶时突然燃起大火,并伴有大量黑烟.某化学小组对电石中碳化钙(CaC2)的性质产生了兴趣,进行了下列探究活动.