题目内容
12. 如图是将等质量的A、B(A、B均为正二价金属)加入到两份质量分数相同且足量的稀盐酸中,产生氢气的质量与反应时间的关系图如图所示,下列说法正确的是( )
如图是将等质量的A、B(A、B均为正二价金属)加入到两份质量分数相同且足量的稀盐酸中,产生氢气的质量与反应时间的关系图如图所示,下列说法正确的是( )| A. | .活动性:A>B | B. | .产生氢气的质量:A<B | ||
| C. | 相对原子质量:A>B | D. | .反应消耗盐酸的量:A<B |
分析 根据等质量的A、B两种金属,活动性强的,与酸反应的速度就快,反应完用的时间就短.所以通过图表中的反应时间我们可判断A、B两种金属的活动性强弱.根据金属与酸反应产生氢气的质量公式:生成氢气的质量=$\frac{金属的化合价}{该金属的相对原子质量}$×金属质量,我们可以比较A、B两种金属相对原子质量的大小进行分析.
解答 解:A、由图象可知A先到达最高点,说明A比B活泼,故A正确;
B、由图象可知产生氢气的质量:A>B,故B错;
C、等质量的A、B(A、B均为正二价金属)加入到两份质量分数相同且足量的稀盐酸中,谁产生的氢气多,谁的相对原子质量小,所以相对原子质量:A<B,故C错;
D、由图象可知产生氢气的质量:A>B,产生的氢气多消耗的酸的质量就多,故D错.
故选A.
点评 解答本题关键是熟悉金属与酸反应的情况分析,并能灵活运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.如图为某化学反应的微观示意图,其中不同的球代表不同种原子.下列说法中正确的是( )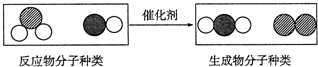

| A. | 此反应属于置换反应 | |
| B. | 化学反应前后分子的种类没有改变 | |
| C. | 原子在化学变化中可分 | |
| D. | 参加反应的两种分子的个数比为1:2 |
7.三氧化二锑(Sb2O3)能与过氧化氢发生如下反应:Sb2O3+2H2O2═X+2H2O,则X的化学式为( )
| A. | Sb2O | B. | SbO3 | C. | Sb2O3 | D. | Sb2O5 |
17.下列物品所使用的主要材料属于有机合成材料的是( )
| A. | 陶瓷花瓶 | B. | 纯棉衣裤 | C. | 塑料桶 | D. | 纳米铜 |
4.下列四个图象分别对应四个变化过程的一种趋势,其说法正确的是( )
?①表示在等质量的铁粉和锌粉中分别加入足量的溶质质量分数相等的稀硫酸
?②用加热一定质量的氯酸钾和二氧化锰固体混合物的方法制取氧气
?③向一定量的硫酸和硫酸铜的混合溶液中逐滴加入一定质量分数的氢氧化钠溶液
④向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化
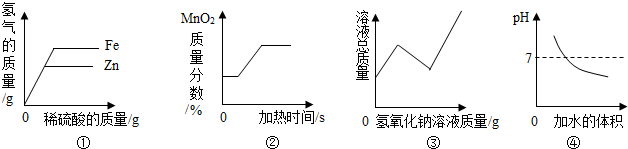
?①表示在等质量的铁粉和锌粉中分别加入足量的溶质质量分数相等的稀硫酸
?②用加热一定质量的氯酸钾和二氧化锰固体混合物的方法制取氧气
?③向一定量的硫酸和硫酸铜的混合溶液中逐滴加入一定质量分数的氢氧化钠溶液
④向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化

| A. | 上述图象只有2个正确 | |
| B. | 上述图象只有3个正确 | |
| C. | 上述图象全部正确 | |
| D. | 如果将②中的纵坐标改为固体总质量,该图象能正确反映相应的变化趋势 |
1.蔗糖的化学式为(C12H22O11),它是食品中常用的甜味剂,下列有关说法正确的是( )
| A. | 蔗糖属于无机化合物 | |
| B. | 蔗糖中氢元素的质量分数最大 | |
| C. | 一个蔗糖分子中有45个原子构成 | |
| D. | 蔗糖中碳、氢、氧元素的质量比为12:22:11 |