题目内容
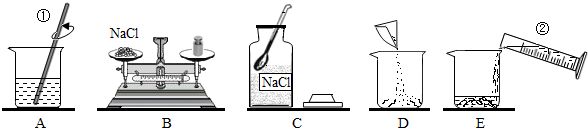
南南同学从家里带了一些鸡蛋壳(鸡蛋壳的主要成分是碳酸钙)到学校的实验室,在老师的指导下,做了如下实验:先用天平称得鸡蛋壳的质量为11g,加入过量的稀盐酸后,发现有大量气泡产生,将生成的气体通过足量的浓的氢氧化钠溶液后,发现氢氧化钠溶液质量增加了4.4g.请你帮她算算:
(1)生成的二氧化碳气体质量
(2)鸡蛋壳中碳酸钙的质量分数(精确到0.1%)
(1)生成的二氧化碳气体质量
(2)鸡蛋壳中碳酸钙的质量分数(精确到0.1%)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,所以氢氧化钠溶液增加的质量就是生成二氧化碳的质量进行解答;
(2)利用二氧化碳质量求出鸡蛋壳中碳酸钙的质量,进而求出鸡蛋壳中碳酸钙的质量分数即可.
(2)利用二氧化碳质量求出鸡蛋壳中碳酸钙的质量,进而求出鸡蛋壳中碳酸钙的质量分数即可.
解答:解:(1)二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,所以氢氧化钠溶液增加的质量就是生成二氧化碳的质量,二氧化碳的质量为4.4g;
(2)设生成4.4g二氧化碳需要碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 4.4g
=
解得x=10g,
该鸡蛋壳中碳酸钙的质量分数:
×100%=90.9%
答:(1)生成的二氧化碳气体质量为4.4g;
(2)鸡蛋壳中碳酸钙的质量分数为90.9%.
(2)设生成4.4g二氧化碳需要碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
解得x=10g,
该鸡蛋壳中碳酸钙的质量分数:
| 10g |
| 11g |
答:(1)生成的二氧化碳气体质量为4.4g;
(2)鸡蛋壳中碳酸钙的质量分数为90.9%.
点评:本题是比较简单的计算题,已知生成物求反应物,需要熟悉比例式的列法,相对分子质量的计算.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
下列各组物质中,属于纯净物的是( )
| A、生铁 | B、天然气 |
| C、冰水 | D、医用酒精 |
按如图提供的信息,以下判断正确的是 ( )
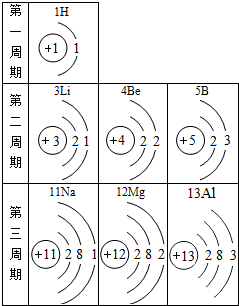

| A、同周期元素的原子最外层电子数相同 |
| B、第二周期中N为金属元素 |
| C、第3号元素的原子容易转变成阴离子 |
| D、Na+和Al3+ 具有相同的核外电子数 |
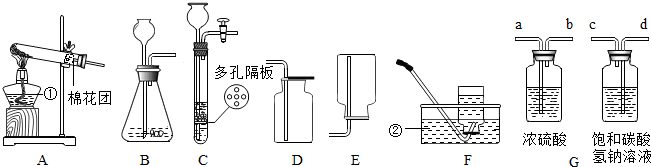
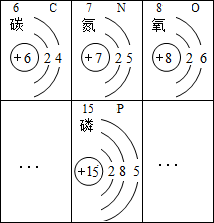 请结合如图回答下列问题:
请结合如图回答下列问题: