题目内容
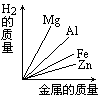
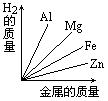
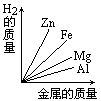
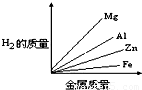
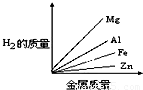
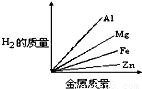
质量相等的镁、铝、锌、铁四种金属分别与足量的硫酸溶液反应,产生氢气的质量与四种金属质量的关系图象(见图),正确的是( )
A.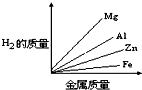 | B.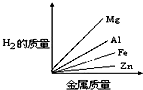 | C.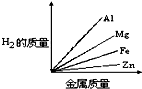 | D.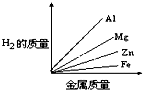 |
设Mg、Fe、Al、Zn的质量为m.生成氢气的质量分别为x、y、z、p
Mg+H2SO4=MgSO4+H2↑
24 2
m x
=
x=
Fe+H2SO4=FeSO4+H2↑
56 2
m y
=
y=
2Al+3H2SO4=Al2(SO4)3+3H2↑
27×2 3×2
m z
=
z=
=
Zn+H2SO4=ZnSO4+H2↑
65 2
m p
=
p=
由此可知等质量的四种金属与酸完全反应放出氢气质量大小为:Al>Mg>Fe>Zn,
故选C.
Mg+H2SO4=MgSO4+H2↑
24 2
m x
| 24 |
| 2 |
| m |
| x |
| 2m |
| 24 |
Fe+H2SO4=FeSO4+H2↑
56 2
m y
| 56 |
| 2 |
| m |
| y |
| 2m |
| 56 |
2Al+3H2SO4=Al2(SO4)3+3H2↑
27×2 3×2
m z
| 27×2 |
| 3×2 |
| m |
| z |
| 6m |
| 54 |
| 2m |
| 18 |
Zn+H2SO4=ZnSO4+H2↑
65 2
m p
| 65 |
| 2 |
| m |
| p |
| 2m |
| 65 |
由此可知等质量的四种金属与酸完全反应放出氢气质量大小为:Al>Mg>Fe>Zn,
故选C.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目