题目内容
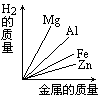
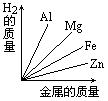
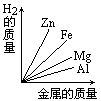
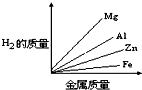
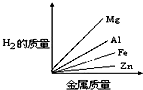
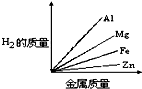
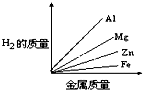
质量相等的镁、铝、锌、铁四种金属分别与足量的硫酸溶液反应,产生氢气的质量与四种金属质量的关系图象(见图),正确的是( )A.
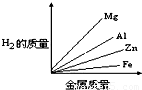
B.
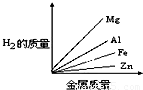
C.
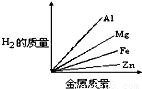
D.

【答案】分析:根据等质量的四种金属与酸完全反应放出氢气质量的大小,判断关系图中四条线与金属的对应关系.
解答:解:设Mg、Fe、Al、Zn的质量为m.生成氢气的质量分别为x、y、z、p
Mg+H2SO4=MgSO4+H2↑
24 2
m x
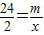 x=
x=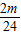
Fe+H2SO4=FeSO4+H2↑
56 2
m y
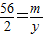 y=
y=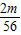
2Al+3H2SO4=Al2(SO4)3+3H2↑
27×2 3×2
m z
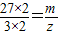 z=
z=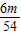 =
=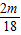
Zn+H2SO4=ZnSO4+H2↑
65 2
m p
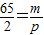 p=
p=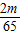
由此可知等质量的四种金属与酸完全反应放出氢气质量大小为:Al>Mg>Fe>Zn,
故选C.
点评:解答本题的关键是会找出等质量的镁、铝、锌、铁与酸完全反应放出氢气的质量由大到小的关系,或找出生成等质量的氢气所需要的四种金属的质量由大到小的关系都可以.
解答:解:设Mg、Fe、Al、Zn的质量为m.生成氢气的质量分别为x、y、z、p
Mg+H2SO4=MgSO4+H2↑
24 2
m x
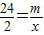 x=
x=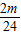
Fe+H2SO4=FeSO4+H2↑
56 2
m y
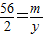 y=
y=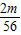
2Al+3H2SO4=Al2(SO4)3+3H2↑
27×2 3×2
m z
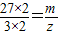 z=
z=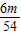 =
=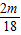
Zn+H2SO4=ZnSO4+H2↑
65 2
m p
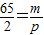 p=
p=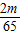
由此可知等质量的四种金属与酸完全反应放出氢气质量大小为:Al>Mg>Fe>Zn,
故选C.
点评:解答本题的关键是会找出等质量的镁、铝、锌、铁与酸完全反应放出氢气的质量由大到小的关系,或找出生成等质量的氢气所需要的四种金属的质量由大到小的关系都可以.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目