��Ŀ����
�����仯��������������������Ҫ��Ӧ�ã���ش��������⣺
��1������Ʒ�ڿ���������ʴ����ʵ������������е������� �ȽӴ�������ѧ��Ӧ�Ĺ��̣�
��2����ʢ�������ļ���ƿ�е�ȼϸ��˿��������ȼ�յĻ�ѧ����ʽ�� ��Ϊ��ֹ����ƿ���ѣ�����ȡ�Ĵ�ʩ�� ��
��3�������ۺ�ͭ�۵Ļ���������������Һ�У���ַ�Ӧ���ˣ�Ϊȷ����������Һ�ijɷ֣���ͬѧ�������еμ�ϡ���ᣬ�����ݲ����� ��ͬѧ����Һ�еμ�ϡ���ᣬ������ɫ������������ͬѧʵ������������н��۲���ȷ���� ����д��ĸ��ţ���
A��������ֻ���� B��������һ�������������ܺ���ͭ
C����Һ��һ����Ag+��Fe2+��Cu2+D����Һ��ֻ��Ag+��Fe2+������Cu2+
��̽����
�Ͼɽ����Ļ������ã�
����м����Ҫ�ɷ�������ͬʱ�����������⣨Fe2O3�������������������Ӽ����������Ĺ���֮һ��ͼ��ʾ��
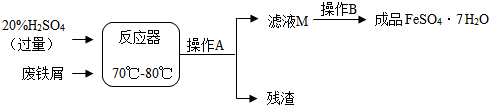
��4���ڷ�Ӧ���з�����Ӧ�Ļ�ѧ����ʽ�У�
Fe+H2SO4=FeSO4+H2���� ��Fe2��SO4��3+Fe=3FeSO4��
��5����ҺM�п϶����е����ʵĻ�ѧʽ�� ��
��6���ڻ�ѧ��Ӧ�У�������Ԫ�ػ��ϼ۱仯�ķ�Ӧ����������ԭ��Ӧ�����з�Ӧ���Ϳ϶�����������ԭ��Ӧ���� ������ĸ��ţ���
A�����Ϸ�ӦB���û���ӦC���ֽⷴӦD�����ֽⷴӦ
��7��ȡ���溬������þ��þ�������������ʣ�2.5g�����뵽������20.0g��ϡ�����У���ַ�Ӧ��������Һ������Ϊ22.3g����þ���е���þ���������������������д�ڴ��ֽ��Ӧ��λ�ã� ��
��1������Ʒ�ڿ���������ʴ����ʵ������������е�������
��2����ʢ�������ļ���ƿ�е�ȼϸ��˿��������ȼ�յĻ�ѧ����ʽ��
��3�������ۺ�ͭ�۵Ļ���������������Һ�У���ַ�Ӧ���ˣ�Ϊȷ����������Һ�ijɷ֣���ͬѧ�������еμ�ϡ���ᣬ�����ݲ����� ��ͬѧ����Һ�еμ�ϡ���ᣬ������ɫ������������ͬѧʵ������������н��۲���ȷ����
A��������ֻ���� B��������һ�������������ܺ���ͭ
C����Һ��һ����Ag+��Fe2+��Cu2+D����Һ��ֻ��Ag+��Fe2+������Cu2+
��̽����
�Ͼɽ����Ļ������ã�
����м����Ҫ�ɷ�������ͬʱ�����������⣨Fe2O3�������������������Ӽ����������Ĺ���֮һ��ͼ��ʾ��

��4���ڷ�Ӧ���з�����Ӧ�Ļ�ѧ����ʽ�У�
Fe+H2SO4=FeSO4+H2����
��5����ҺM�п϶����е����ʵĻ�ѧʽ��
��6���ڻ�ѧ��Ӧ�У�������Ԫ�ػ��ϼ۱仯�ķ�Ӧ����������ԭ��Ӧ�����з�Ӧ���Ϳ϶�����������ԭ��Ӧ����
A�����Ϸ�ӦB���û���ӦC���ֽⷴӦD�����ֽⷴӦ
��7��ȡ���溬������þ��þ�������������ʣ�2.5g�����뵽������20.0g��ϡ�����У���ַ�Ӧ��������Һ������Ϊ22.3g����þ���е���þ���������������������д�ڴ��ֽ��Ӧ��λ�ã�
���㣺������ʴ�������������,�����Ļ�ѧ����,���ʵ��ת�����Ʊ�,������Ӧ,��ԭ��Ӧ,���ݻ�ѧ��Ӧ����ʽ�ļ���
ר�⣺�йػ�ѧ����ʽ�ļ���,�������������
��������1��������������������
��2��������˿��������ȼ����������������������ƿ��Ҫ��������ˮ��ϸɳ��ֹը�Ѽ���ƿ���
��3���������ֽ������ǿ����ϵ����ͭ�������Խ����ۺ�ͭ�۵Ļ���������������Һ�п��ܳ��ֵı仯���з������жϷ�Ӧ������ʣ�����ɷ֣�
��4���������������ܺ�ϡ���ᷴӦ�����Ծݴ�д����Ӧ�Ļ�ѧ����ʽ��
��5������������ǹ����ģ���������Һ�к�������ͷ�Ӧ���ɵ��������������Ծݴ˽����⣻
��6���������ֻ�����Ӧ���͵��ص��������⣻
��7�����������غ㶨�����������������Ȼ�����þ��ϡ���ᷴӦ�Ļ�ѧ����ʽ����þ���������
��2��������˿��������ȼ����������������������ƿ��Ҫ��������ˮ��ϸɳ��ֹը�Ѽ���ƿ���
��3���������ֽ������ǿ����ϵ����ͭ�������Խ����ۺ�ͭ�۵Ļ���������������Һ�п��ܳ��ֵı仯���з������жϷ�Ӧ������ʣ�����ɷ֣�
��4���������������ܺ�ϡ���ᷴӦ�����Ծݴ�д����Ӧ�Ļ�ѧ����ʽ��
��5������������ǹ����ģ���������Һ�к�������ͷ�Ӧ���ɵ��������������Ծݴ˽����⣻
��6���������ֻ�����Ӧ���͵��ص��������⣻
��7�����������غ㶨�����������������Ȼ�����þ��ϡ���ᷴӦ�Ļ�ѧ����ʽ����þ���������
����⣺��1�����ڳ�ʪ�Ŀ������������⼴����������ˮͬʱ�Ӵ������⣻
��2����˿��������ȼ����������������������ƿ��Ҫ��������ˮ��ϸɳ��ֹը�Ѽ���ƿ��
��3���������ֽ������ǿ����ϵ����ͭ�����������ۺ�ͭ�۵Ļ���������������Һ�У����ۡ�ͭ�۶�����������������Ӧ�õ��������ʣ�������һ������������ͬѧ�������еμ�ϡ���ᣬ�����ݲ�����˵����ȫ����Ӧ����ͬѧ����Һ�еμ�ϡ���ᣬ������ɫ������˵����Һ�к��������������Կ�ȷ��ͭ����������Ӧ��ͭ�������㻹��������û��Ӧ��������������Ӧ������������������ͭ����������Ӧ��������ͭ�������������ù�����ֻ��������������Һ�к����������ӡ�ͭ���Ӻ������ӣ�����BD˵������ȷ��
��4�����������ܺ�ϡ���ᷴӦ��������������������������Ӧ��������������ˮ����Ӧ�Ļ�ѧ����ʽΪFe2O3+3H2SO4=Fe2��SO4��3+3H2O��
��5������������ǹ����ģ���������Һ�к�������ͷ�Ӧ���ɵ�����������
��6���������ֻ�����Ӧ���͵��ص����֪�������û���Ӧ���е��ʲ���������µĵ��ʣ����Կ����ж����û���Ӧ��һ���л��ϼ۵ı仯����ѡB��
��7���裺2.5gþ����Ʒ�е���þ������Ϊx
��Ӧ����������������2.5g+20.0g-22.3g=0.2g
Mg+H2SO4=MgSO4+H2��
24 2
X 0.2g
=
x=2.4g
��þ���е���þ����������=
��100%=96%
�𣺸�þ���е���þ����������Ϊ96%��
�ʴ𰸣���1��ˮ����ˮ������H2O������2��3Fe+2O2
Fe3O4���ڼ���ƿ������ˮ����ɳ�ӣ�����3��BD����4��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O
����5��FeSO4��H2SO4����6��B����7��96%��
��2����˿��������ȼ����������������������ƿ��Ҫ��������ˮ��ϸɳ��ֹը�Ѽ���ƿ��
��3���������ֽ������ǿ����ϵ����ͭ�����������ۺ�ͭ�۵Ļ���������������Һ�У����ۡ�ͭ�۶�����������������Ӧ�õ��������ʣ�������һ������������ͬѧ�������еμ�ϡ���ᣬ�����ݲ�����˵����ȫ����Ӧ����ͬѧ����Һ�еμ�ϡ���ᣬ������ɫ������˵����Һ�к��������������Կ�ȷ��ͭ����������Ӧ��ͭ�������㻹��������û��Ӧ��������������Ӧ������������������ͭ����������Ӧ��������ͭ�������������ù�����ֻ��������������Һ�к����������ӡ�ͭ���Ӻ������ӣ�����BD˵������ȷ��
��4�����������ܺ�ϡ���ᷴӦ��������������������������Ӧ��������������ˮ����Ӧ�Ļ�ѧ����ʽΪFe2O3+3H2SO4=Fe2��SO4��3+3H2O��
��5������������ǹ����ģ���������Һ�к�������ͷ�Ӧ���ɵ�����������
��6���������ֻ�����Ӧ���͵��ص����֪�������û���Ӧ���е��ʲ���������µĵ��ʣ����Կ����ж����û���Ӧ��һ���л��ϼ۵ı仯����ѡB��
��7���裺2.5gþ����Ʒ�е���þ������Ϊx
��Ӧ����������������2.5g+20.0g-22.3g=0.2g
Mg+H2SO4=MgSO4+H2��
24 2
X 0.2g
| 24 |
| x |
| 2 |
| 0.2g |
x=2.4g
��þ���е���þ����������=
| 2.4g |
| 2.5g |
�𣺸�þ���е���þ����������Ϊ96%��
�ʴ𰸣���1��ˮ����ˮ������H2O������2��3Fe+2O2
| ||
����5��FeSO4��H2SO4����6��B����7��96%��
���������ջ�ѧ����ʽ����д���εĻ�ѧ���ʵ�֪ʶ����ѧ�������Ϣ����ȡ��Ϣ����Ӧ����ѧ֪ʶ���������Ϣ���н�𣬿�����ѧ����������������������

��ϰ��ϵ�д�
 ��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
�����Ŀ
���в�������������ǣ�������
| A���������� | B������������ |
| C��������� | D���������� |
3A+B�T2C����֪�μӷ�Ӧ��A��B��������Ϊ3��4����һ������A��������B��Ӧ����21��C����μӷ�Ӧ��B������Ϊ��������
| A��6�� | B��8 �� |
| C��12�� | D��4�� |
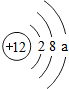 ����a��ֵΪ
����a��ֵΪ