题目内容
15.某实验室取来一些卤块样品,其成分是氯化镁和氯化钠的固体混合物,称取不同质量的该混合物样品与不同质量的溶质质量分数相同的氢氧化钠溶液混合,充分振荡,实验所得数据如表,请你分析并进行有关计算:| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 卤块样品质量/g | 6 | 12 | 12 | 18 | 12 |
| 氢氧化钠溶液质量/g | 58 | 29 | 58 | 58 | 87 |
| 生成沉淀质量/g | 2.9 | 2.9 | 5.8 | 5.8 | 5.8 |
(2)卤块样品中氯化镁的质量分数为79.2%.(结果保留小数点后一位)
(3)已知20℃NaCl的溶解度为36g,用上述实验中氯化镁与氢氧化钠恰好完全反应的溶液,温度调至20℃,配制成该温度时的NaCl饱和溶液,还需加入氯化钠多少g?(写出计算过程)
分析 氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)由表中数据可知,1中氢氧化钠溶液过量,2中卤块样品过量,4中卤块样品过量,5中氢氧化钠溶液过量,3中恰好完全反应.
故填:3.
(2)设样品中氯化镁质量为x,氢氧化钠质量为y,生成氯化钠质量为z,
MgCl2+2NaOH═Mg(OH)2↓+2NaCl,
95 80 58 117
x y 5.8g z
$\frac{95}{x}$=$\frac{80}{y}$=$\frac{58}{5.8g}$=$\frac{117}{z}$,
x=9.5g,y=8g,z=11.7g,
卤块样品中氯化镁的质量分数为:$\frac{9.5g}{12g}$×100%=79.2%,
故填:79.2%.
(3)配制成该温度时的NaCl饱和溶液,还需加入氯化钠的质量为:$\frac{(58g-8g)×36g}{100g}$-11.7g-(12g-9.5g)=3.8g,
答:配制成该温度时的NaCl饱和溶液,还需加入氯化钠的质量是3.8g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
7.探究镁和锌与盐酸反应的快慢,不需要控制的变量是( )
| A. | 两种金属的形状 | B. | 盐酸的质量分数 | C. | 温度 | D. | 反应容器的大小 |
3.下列变化中,属于化学变化的是( )
| A. | 干冰升华 | B. | 蜡烛燃烧 | C. | 活性炭吸附色素 | D. | 矿石粉碎 |
10.如图圆圈分别表示物质R的类别、性质与用途,则R物质可能是( )
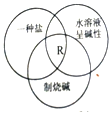

| A. | 食盐 | B. | 碳酸钙 | C. | 碳酸钠 | D. | 氢氧化钙 |
20.鸡蛋壳的主要成分是碳酸钙.某校化学兴趣小组同学为了测定鸡蛋壳中碳酸钙的含量,将80克稀盐酸加入到12克干燥的碎鸡蛋壳中充分反应(杂质不与盐酸反应).产生气体的质量(m)与反应时间(t)的如表所示.
(1)完全反应后,生成CO2的质量为4.4g.
(2)请在如图的坐标图中,画出反应时生成气体的质量(m)随时间(t)变化的曲线.
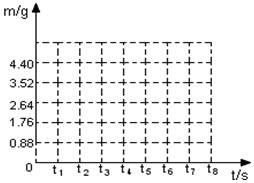
(3)求该鸡蛋壳中碳酸钙的质量分数.
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
(2)请在如图的坐标图中,画出反应时生成气体的质量(m)随时间(t)变化的曲线.

(3)求该鸡蛋壳中碳酸钙的质量分数.
7.酸、碱、盐溶解性表是学习自然科学的重要工具,下表列出了“部分酸、碱、盐在20℃时的溶解性”.请利用此表完成下列任务:
(1)查Mg(OH)2的溶解性:不溶(填“溶”或“不溶”).
(2)用化学方程式表示CuSO4与表中的一种碱的溶液反应2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
| OH- | Cl- | CO32- | SO42- | |
| H+ | 溶、挥 | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Mg2+ | 不溶 | 溶 | 不溶 | 溶 |
| Cu2+ | 不溶 | 溶 | 不溶 | 溶 |
(2)用化学方程式表示CuSO4与表中的一种碱的溶液反应2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
4.以下是根据一些反应事实推理出的影响化学反应的因素,其中推理不合理的是( )
| A. | 双氧水在常温下很难分解,而在加入二氧化锰后迅速分解--催化剂 | |
| B. | 硫在空气中燃烧发出淡蓝色火焰,在纯氧中燃烧发出蓝紫色火焰--反应物浓度 | |
| C. | 食物在冰箱中保存不易腐烂--温度 | |
| D. | 铜片在空气中很难燃烧,铜粉在空气中能燃烧--反应物的种类 |
 (1)葡萄糖中C、H原子个数比为1:2.
(1)葡萄糖中C、H原子个数比为1:2.