题目内容
4.对于钠原子Na和钠离子Na+两种粒子的判断中,正确的是( )①核电荷数相同 ②化学性质相同 ③电子数相同 ④质量几乎相等.
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ①②③④ |
分析 根据Na为钠原子,Na+为钠离子,两种粒子的质子数(等于核电荷数)相等,属于同种元素;钠原子失去1个电子形成Na+,电子的质量很小,可以忽略不计;进行解答.
解答 解:
①根据Na为钠原子,Na+为钠离子,属于同种元素,因此两种粒子的核电荷数相等,故说法正确;
②根据钠原子的最外层电子数是1,钠离子的最外层电子数是8,两种粒子的化学性质不相同,故说法错误;
③钠原子Na失去1个电子形成Na+,因此它们的核外电子数不相等;故说法不正确;
④钠原子Na失去1个电子形成Na+,电子的质量很小,可以忽略不计;因此Na和Na+质量几乎相等;故说法正确;
故选C.
点评 本题考查学生对构成物质的基本微粒原子与离子的构成与相互转换,及其同异.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.有一种无色液体,不能使紫色石蕊试液变色,与AgNO3生成不溶于稀HNO3的白色沉淀,这无色溶液是( )
| A. | NaCl | B. | H2O | C. | HCl | D. | NaOH |
19.根据下面的粒子结构示意图回答问题
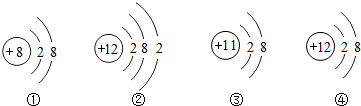
(1)属于原子的是②;
(2)属于阳离子的是③④;
(3)属于阴离子的是①;
(4)属于同种元素的是③④;
(5)具有相似化学性质的是③④;
(6)达到稳定结构的是①③④.

(1)属于原子的是②;
(2)属于阳离子的是③④;
(3)属于阴离子的是①;
(4)属于同种元素的是③④;
(5)具有相似化学性质的是③④;
(6)达到稳定结构的是①③④.
9.小丽在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地看到有气泡产生,她认为氢氧化钠溶液已经变质了.请用化学方程式表示氢氧化钠溶液变质的原因:CO2+2NaOH=Na2CO3+H2O
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:氢氧化钠和碳酸钠; 猜想二:只有碳酸钠.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化.小林认为小丽的实验方案不合理,理由是:碳酸钠的水溶液呈碱性,能使无色酚酞溶液变红
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:氢氧化钠和碳酸钠; 猜想二:只有碳酸钠.
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化.小林认为小丽的实验方案不合理,理由是:碳酸钠的水溶液呈碱性,能使无色酚酞溶液变红
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量氢氧化钠溶液样品于试管中, 向其中滴加足量的CaCl2溶液 | 有白色沉淀生成 | 猜想一 正确 |
| 步骤2:将步骤1试管中的混合物过滤,向滤液中滴加无色酚酞溶液 | 溶液变红 |
13.20世纪初,一些化学家提出了酸碱质子理论.这种理论认为,凡能放出质子(H+)的分子或离子都是酸;凡能结合质子的分子或离子都是碱.根据这一理论,下列物质中既属于酸又属于碱的是( )
| A. | HNO3 | B. | HCO3- | C. | NH4+ | D. | SO42- |
14.下列叙述不正确的是( )
| A. | 缓慢氧化和燃烧都是氧化反应 | B. | 爆炸都是化学变化 | ||
| C. | 铁丝不能在空气中燃烧 | D. | 油锅着时应立即盖上锅盖 |
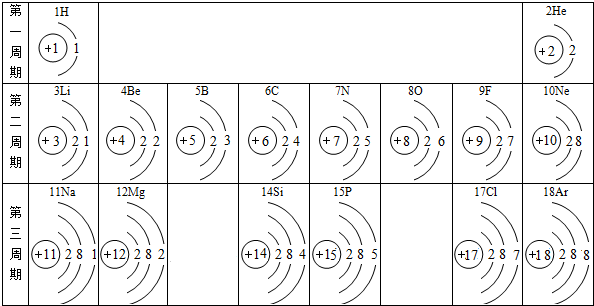
 化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子;
化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子;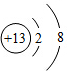 表示的是Al3+(填离子符号);
表示的是Al3+(填离子符号);

