题目内容
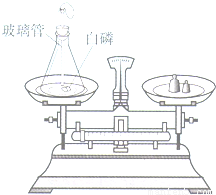
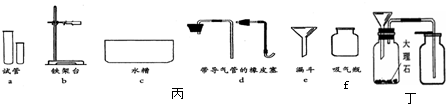
某化学兴趣小组利用下图装置进行质量守恒定律的探究.(1)锥形瓶底部放一些细沙的目的是______;
(2)锥形瓶中的现象是______,
反应的化学方程式为______ 2P2O5
【答案】分析:质量守恒定律的内容是:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和.本实验成功的关键是:①白磷过量②锥形瓶的气密性好③冷却到室温再读数.因此过量的白磷又与空气中的氧气接触后继续燃烧,这样密闭系统打破,天平就不平衡了.可以根据化学方程式的计算,得到氧气的质量.
解答:解:(1)白磷燃烧放热,防止炸裂锥形瓶.故答案为:防止燃烧时放出的大量热使锥形瓶破裂;
(2)锥形瓶内白磷燃烧生成五氧化二磷,产生大量白烟,化学方程式为:4P+5O2 2 P2O5
2 P2O5
(3)开始燃烧时,反应放出的大量热,使密闭体系内的空气受热膨胀,气球变大;反应结束后,锥形瓶内的氧气被消耗,使密闭体系内的压强减小(P2O5常温下是固体),导致气球变小.
(4)白磷又燃烧是因为白磷过量,打开橡胶塞后,白磷又与空气中的氧气接触后继续燃烧,这时天平就不平衡了.故答案为:没有反应完的白磷与空气中的氧气接触后继续燃烧;不平衡;
(5)氧气的相对分子质量=16×2=32
设氧气的质量为x,
4P+5O2 2 P2O5
2 P2O5
4×31 5×32
3.1g x
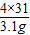 =
=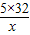
x=4g
故答案为:4
(6)白磷露置在空气中极易自燃,随意放置或丢弃容易引发火灾,当实验结束后,锥形瓶中剩余的白磷,可以在通风厨中用酒精灯灼烧掉.
故答案为:
(1)防止燃烧时放出的大量热使锥形瓶破裂;
(2)白磷燃烧,产生大量白烟,4P+5O2 2 P2O5;
2 P2O5;
(3)开始燃烧时,反应放出的大量热,使密闭体系内的空气受热膨胀,气球变大;反应结束后,锥形瓶内的氧气被消耗,使密闭体系内的压强减小(P2O5常温下是固体),导致气球变小.
(4)没有反应完的白磷与空气中的氧气接触后继续燃烧;不平衡;
(5)32;4;
(6)在通风厨中用酒精灯灼烧掉.
点评:本考点考查了有关质量守恒定律的实验探究和有关化学方程式的计算,质量守恒定律是一个实验结论,要抓住元素守恒和原子守恒,本考点主要出现在实验题和计算题中.
解答:解:(1)白磷燃烧放热,防止炸裂锥形瓶.故答案为:防止燃烧时放出的大量热使锥形瓶破裂;
(2)锥形瓶内白磷燃烧生成五氧化二磷,产生大量白烟,化学方程式为:4P+5O2
 2 P2O5
2 P2O5 (3)开始燃烧时,反应放出的大量热,使密闭体系内的空气受热膨胀,气球变大;反应结束后,锥形瓶内的氧气被消耗,使密闭体系内的压强减小(P2O5常温下是固体),导致气球变小.
(4)白磷又燃烧是因为白磷过量,打开橡胶塞后,白磷又与空气中的氧气接触后继续燃烧,这时天平就不平衡了.故答案为:没有反应完的白磷与空气中的氧气接触后继续燃烧;不平衡;
(5)氧气的相对分子质量=16×2=32
设氧气的质量为x,
4P+5O2
 2 P2O5
2 P2O5 4×31 5×32
3.1g x
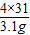 =
=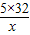
x=4g
故答案为:4
(6)白磷露置在空气中极易自燃,随意放置或丢弃容易引发火灾,当实验结束后,锥形瓶中剩余的白磷,可以在通风厨中用酒精灯灼烧掉.
故答案为:
(1)防止燃烧时放出的大量热使锥形瓶破裂;
(2)白磷燃烧,产生大量白烟,4P+5O2
 2 P2O5;
2 P2O5;(3)开始燃烧时,反应放出的大量热,使密闭体系内的空气受热膨胀,气球变大;反应结束后,锥形瓶内的氧气被消耗,使密闭体系内的压强减小(P2O5常温下是固体),导致气球变小.
(4)没有反应完的白磷与空气中的氧气接触后继续燃烧;不平衡;
(5)32;4;
(6)在通风厨中用酒精灯灼烧掉.
点评:本考点考查了有关质量守恒定律的实验探究和有关化学方程式的计算,质量守恒定律是一个实验结论,要抓住元素守恒和原子守恒,本考点主要出现在实验题和计算题中.

练习册系列答案
相关题目



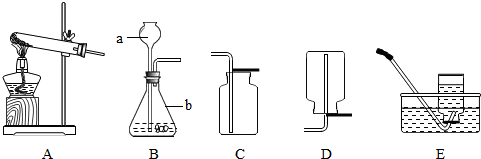
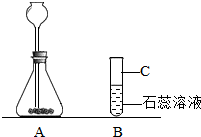
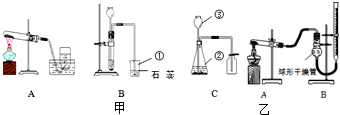
 (2007?莆田)某化学兴趣小组利用如图装置进行饱和NaCl溶液的电解实验,并对部分产物进行探究.
(2007?莆田)某化学兴趣小组利用如图装置进行饱和NaCl溶液的电解实验,并对部分产物进行探究.