题目内容
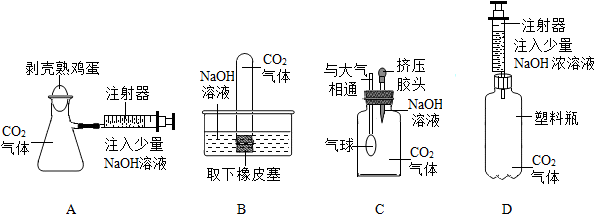
5.下列是按设计能达到的实验目的是( )| A. |  探究反应物浓度对反应速度的影响 | B. |  探究可燃物燃烧的两个条件 | ||
| C. |  证明CH4燃烧生成二氧化碳和水 | D. |  验证质量守恒定律 |
分析 反应物浓度不同,反应速率不同;
可燃物燃烧的条件是:与氧气接触,温度达到着火点;
甲烷燃烧生成水和二氧化碳;
化学反应遵循质量守恒定律.
解答 解:A、锌与不同浓度的反应物反应时,反应速率不同,因此实验现象不同,该选项能够达到实验目的;
B、白磷燃烧,红磷不能燃烧,说明燃烧需要温度达到着火点,不能说明燃烧需要氧气,该选项不能达到实验目的;
C、实验过程中,澄清石灰水变浑浊,说明燃烧产生了二氧化碳,不能说明燃烧生成水,该选项不能达到实验目的;
D、碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,生成的二氧化碳逸散到空气中,不能验证质量守恒定律,该选项不能达到实验目的.
故选:A.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
15.甲、乙、丙、丁四位同学用锌与稀硫酸反应,所得相关数据记录如下(实验中的误差忽略不计),计算:
(1)写出锌与稀硫酸反应的化学方程式Zn+H2SO4═ZnSO4+H2↑
(2)甲同学加入金属锌的质量X是多少?
(3)稀硫酸中溶质的质量分数是多大?
| 甲 | 乙 | 丙 | 丁 | |
| 取用稀硫酸质量/克 | 100 | 100 | 100 | 200 |
| 加入金属锌的质量/克 | X | 1.25x | 2x | 2x |
| 生成氢气的质量/克 | 0.4 | 0.5 | 0.6 | 0.8 |
(2)甲同学加入金属锌的质量X是多少?
(3)稀硫酸中溶质的质量分数是多大?