题目内容
18.碳酸亚铁(FeCO3)是生产补血剂的原料.下图是利用铁矿烧渣(主要成分是Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图: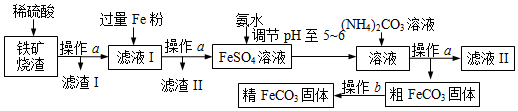
(1)操作a中用到的玻璃仪器主要有烧杯、玻璃棒和漏斗.
(2)滤液I中加入铁粉一段时间后有气泡产生,产生气泡的化学方程式:Fe+H2SO4=FeSO4+H2↑.
(3)“调节pH至5~6”时可用pH试纸或者pH计测定加入氨水后溶液的pH.
(4)操作b为洗涤、低温干燥,判断FeCO3固体已洗涤干净的方法是:取最后一次洗涤后的过滤液,滴加氯化钡溶液,无沉淀产生.
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
(1)操作a得到的结果是滤液和滤渣,所以应该是过滤,所用到的玻璃仪器主要有烧杯、玻璃棒和 漏斗.
(2)由于为使铁矿烧渣中所含铁元素尽可能完全进入溶液,所以加入的稀硫酸时过量的,所以对应的有气泡产生的反应是铁和稀硫酸反应生成硫酸亚铁和氢气,对应的化学方程式为:Fe+H2SO4=FeSO4+H2↑.
(3)由于测定pH变化情况,所以“调节pH至5~6”时可用pH试纸或者pH计测定加入氨水后溶液的pH.
(4)得到的粗碳酸亚铁是硫酸亚铁和碳酸铵生成的碳酸亚铁和硫酸铵,所以得到的碳酸亚铁表面会附着硫酸铵,所以操作b为洗涤、低温干燥中,判断FeCO3固体已洗涤干净就是看洗涤后碳酸亚铁表面是否附着硫酸铵,也就是检验硫酸根或者是铵根的存在,由于此时铵根量很小,通过检验铵根的现象不明显,不适宜进行判断.所以可以借助检验硫酸根生成硫酸钡沉淀的现象进行,所以取最后一次洗涤后的过滤液,滴加氯化钡溶液,由于是结论是已经洗涤干净,所以对应的现象是无沉淀产生.
故答案为:
(1)漏斗.
(2)Fe+H2SO4=FeSO4+H2↑.
(3 )pH试纸或者pH计.
(4)滴加氯化钡溶液,无沉淀产生
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.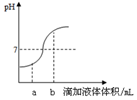 如图是盐酸和氢氧化钙溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列有关说法正确的是( )
如图是盐酸和氢氧化钙溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列有关说法正确的是( )
 如图是盐酸和氢氧化钙溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列有关说法正确的是( )
如图是盐酸和氢氧化钙溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.下列有关说法正确的是( )| A. | 该图象表示的是将稀盐酸滴入氢氧化钙溶液中 | |
| B. | 当滴入溶液的体积为amL时,所得溶液中的溶质只有CaCl2 | |
| C. | 滴入溶液体积为bmL时,再加几滴酚酞试液溶液呈红色 | |
| D. | 恰好完全反应后溶液中存在的粒子只有Ca2+和Cl-离子 |
9.下列变化中与其他之间有着本质区别的是( )
| A. | 煤的干馏 | B. | 百炼成钢 | C. | 石油分馏 | D. | 蜡烛燃烧 |
6.下列排列顺序正确的是( )
| A. | 氯元素的化合价: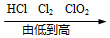 | B. | 溶于水后的水温: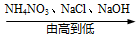 | C. | 地壳中元素含量: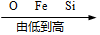 | D. | 铁元素质量分数: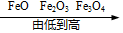 |
13.如图是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )
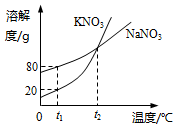

| A. | t1℃时,两物质的溶液溶质质量分数一定不等 | |
| B. | t1℃时,50g水里加入15g KNO3固体,充分溶解,得到60g溶液 | |
| C. | t1℃时,两物质饱和溶液升温到t2℃后,溶质质量分数:NaNO3=KNO3 | |
| D. | 两种物质饱和溶液从t2℃降温到t1℃时,析出晶体的质量:KNO3>NaNO3 |
3.砷化镓(GaAs)是制造光源LED 的材料.其中As是-3价,则Ga化合价为( )
| A. | +3 | B. | +5 | C. | -3 | D. | -5 |
10.水是生命之源,我们应该了解水、爱护水资源.下列说法错误的是( )
| A. | 净水的方法通常有沉淀、过滤、吸附和蒸馏 | |
| B. | 自来水厂常用ClO2消毒,ClO2中氯元素的化合价为+4 | |
| C. | 通过过滤的方法可以将不溶于水的固体杂质与水分离开来 | |
| D. | 电解水时,产生氢气、氧气的体积比为1:2,质量比为1:8. |
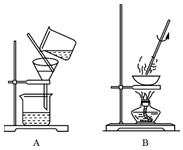 实验室有如图所示装置,回答下列问题:
实验室有如图所示装置,回答下列问题: