题目内容
13.如图是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )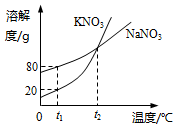
| A. | t1℃时,两物质的溶液溶质质量分数一定不等 | |
| B. | t1℃时,50g水里加入15g KNO3固体,充分溶解,得到60g溶液 | |
| C. | t1℃时,两物质饱和溶液升温到t2℃后,溶质质量分数:NaNO3=KNO3 | |
| D. | 两种物质饱和溶液从t2℃降温到t1℃时,析出晶体的质量:KNO3>NaNO3 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、因为不知道溶液的状态,故t1℃时,两物质的溶液溶质质量分数不一定相等,错误;
B、据图可以看出,在t1℃时,硝酸钾的溶解度为20g,50g水里加入15g KNO3固体,充分溶解,只能溶解10g,故得到60g溶液,正确;
C、t1℃时,两物质饱和溶液升温到t2℃后,溶液组成不变,故溶质质量分数:NaNO3>KNO3,错误;
D、因为不知道溶液的质量,故两种物质饱和溶液从t2℃降温到t1℃时,析出晶体的质量无法确定,错误;
故选B.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列化学用语中,既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | O2 | B. | H | C. | Cu | D. | SO2 |
1.下列化学用语或对化学用语表述正确的是( )
| A. | 氧化铝--AlO | B. | 2个水分子--2H2O | ||
| C. | SO2--二氧化硫中有氧分子 | D. | Fe2+--铁离子带2个单位的正电荷 |
8.下列化学方程式与实际相符,且书写正确的是( )
| A. | 铁丝在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 洗去试管壁上附着的铜:Cu+H2SO4=CuSO4+H2↑ | |
| C. | 用氢氧化钠溶液吸收二氧化硫:2NaOH+SO2=Na2SO4+H2O | |
| D. | 用氢氧化镁中和过多胃酸:Mg(OH)2+2HCl=MgCl2+2H2O |
5.屠呦呦由于发现青蒿素获得诺贝尔奖.关于青蒿素(C15H22O5)正确的是( )
| A. | 是氧化物 | B. | 相对分子质量302克 | ||
| C. | 有42个原子 | D. | 碳元素质量分数最大 |
3.某同学用pH 试纸测得以下液体的pH,实验过程中pH 试纸变成蓝色的是( )
| A. | 雨水pH=6 | B. | 食醋pH=3 | C. | 肥皂水pH=10 | D. | 食盐水pH=7 |