题目内容
7.兴趣小组同学发现实验室一片久置的铜片表面附着有一层绿色固体,查阅资料得知绿色是铜绿[化学式为Cu2(OH)2CO3],能与稀硫酸反应产生硫酸铜、水和二氧化碳,加热产生氧化铜、水和二氧化碳.下面是小组同学回收铜的实验流程: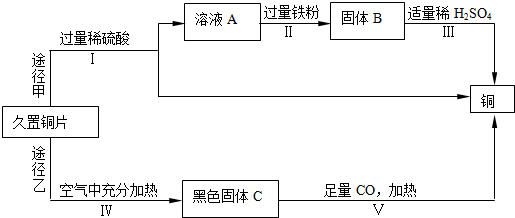
回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ都需要进行过滤的操作,过滤用到的玻璃仪器是烧杯、玻璃棒和漏斗.溶液A所含的溶质有H2SO4、CuSO4(填化学式)
(2)写出下列反应的化学方程式:步骤ⅡFe+CuSO4═FeSO4+Cu,H2SO4+Fe═FeSO4+H2↑,步骤ⅢH2SO4+Fe═FeSO4+H2↑.
(3)同一久置铜片分别通过途径甲和途径乙最终得到的铜的质量是:途径甲等于(选填“大于”、“等于”或“小于”)途径乙.
(4)途径甲比途径乙更好的理由是节能环保(答一点).
分析 (1)过滤能够把固体和液体分离,用到的玻璃仪器是烧杯、玻璃棒和漏斗;
溶液A所含的溶质有过量的硫酸和反应生成的硫酸铜;
(2)步骤Ⅱ中,铁和硫酸铜反应生成硫酸亚铁和铜,和稀硫酸反应生成硫酸亚铁和氢气;
步骤Ⅲ中,过量的铁和稀硫酸反应生成硫酸亚铁和氢气;
(3)同一久置铜片分别通过途径甲和途径乙时,铜元素没有流失,因此最终得到的铜的质量是:途径甲等于途径乙;
(4)途径甲比途径乙更好的理由是不需要加热,不使用有毒物质例如一氧化碳等.
解答 解:(1)Ⅰ、Ⅱ、Ⅲ都需要进行过滤的操作,过滤用到的玻璃仪器是烧杯、玻璃棒和漏斗;
溶液A所含的溶质有过量的硫酸和反应生成的硫酸铜.
故填:漏斗; H2SO4、CuSO4.
(2)步骤Ⅱ中,铁和硫酸铜反应生成硫酸亚铁和铜,和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu,H2SO4+Fe═FeSO4+H2↑;
步骤Ⅲ中,过量的铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:H2SO4+Fe═FeSO4+H2↑.
故填:Fe+CuSO4═FeSO4+Cu,H2SO4+Fe═FeSO4+H2↑;H2SO4+Fe═FeSO4+H2↑.
(3)同一久置铜片分别通过途径甲和途径乙时,铜元素没有流失,因此最终得到的铜的质量是:途径甲等于途径乙.
故填:等于.
(4)途径甲比途径乙更好的理由是不需要加热,不使用有毒物质例如一氧化碳等,因此途径甲比途径乙更好的理由是 节能环保.
故填:节能环保.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
6.CO2是重要的资源,以其为原料可获得下列四种物质.下列说法错误的是( )
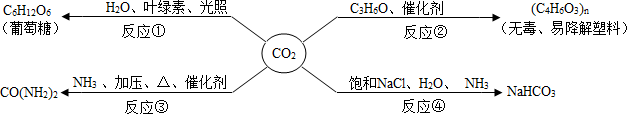

| A. | 反应①是太阳能转化为化学能 | |
| B. | 反应②的实现有利于缓解“白色污染” | |
| C. | 反应③可用来制取氮肥 | |
| D. | 反应④获得产品后的剩余液中,溶质只有NaHCO3 |
4.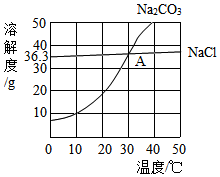 如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A.下列说法正确的是( )
如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A.下列说法正确的是( )
 如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A.下列说法正确的是( )
如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A.下列说法正确的是( )| A. | 碳酸钠俗称小苏打 | |
| B. | 30℃时,氯化钠的溶解度为36.3g | |
| C. | 碳酸钠的溶解度大于氯化钠的溶解度 | |
| D. | 将Na2CO3和NaCl均达到饱和的混合溶液,从40℃降温到20℃时,析出的固体物质主要是NaCl |
12.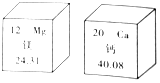 俗话说:“补钙不补镁,补了也后悔”,原来镁有协同钙的作用,会促进钙的吸收.如图是镁、钙在元素周期表中的部分信息,则下列说法不正确的是( )
俗话说:“补钙不补镁,补了也后悔”,原来镁有协同钙的作用,会促进钙的吸收.如图是镁、钙在元素周期表中的部分信息,则下列说法不正确的是( )
 俗话说:“补钙不补镁,补了也后悔”,原来镁有协同钙的作用,会促进钙的吸收.如图是镁、钙在元素周期表中的部分信息,则下列说法不正确的是( )
俗话说:“补钙不补镁,补了也后悔”,原来镁有协同钙的作用,会促进钙的吸收.如图是镁、钙在元素周期表中的部分信息,则下列说法不正确的是( )| A. | 镁和钙都属于金属元素 | B. | 在金属活动性顺序中,镁比钙活泼 | ||
| C. | 镁原子的质子数为12 | D. | 钙的相对原子质量为40.08 |
16.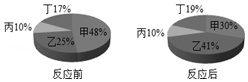 在密闭容器中有甲、乙、丙、丁四种物质,在一定的条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
在密闭容器中有甲、乙、丙、丁四种物质,在一定的条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
 在密闭容器中有甲、乙、丙、丁四种物质,在一定的条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
在密闭容器中有甲、乙、丙、丁四种物质,在一定的条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )| A. | 丁一定是化合物 | B. | 丙一定是这个反应的催化剂 | ||
| C. | 该反应一定是分解反应 | D. | 该反应可能是碳酸钙的分解 |
17.我国科学家屠呦呦及她的团队发现了青蒿素,并运用在医学上,是治疗疟疾的特效药,获得了诺贝尔奖.青蒿素化学式为 C15H22O5,关于青篙素的说法正确的是( )
| A. | 不属于有机物 | |
| B. | C15H22O5中碳元素的质量分数是$\frac{12×5}{12×15+1×22+16×5}$×100% | |
| C. | 一个青篙素分子含有 11 个氢分子 | |
| D. | C、H、O 三种元素的质量比为 15:22:5 |
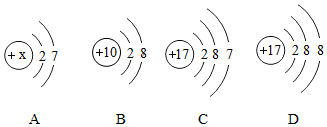 根据下图提供的信息,请回答下列问题:
根据下图提供的信息,请回答下列问题: