题目内容
17.你注意过吗?家庭使用的铁制工具隔一段时间不用就变得锈迹斑斑,而街心广场矗立的不锈钢雕塑,几经风霜雨雪总能保持原有的本色.锰(Mn)就是不锈钢的主要添加元素之一,它可以提高不锈钢的耐腐蚀性.(1)铁与空气中的水和氧气直接接触会导致铁制品的锈蚀.
(2)不锈钢属于B(填序号).
A.纯净物 B.金属材料 C.合成材料 D.复合材料
(3)某化学兴趣小组的同学为了探究锰、镁、铜三种金属的活动性,他们首先将锰片插入到氯化镁溶液中,一段时间后,观察到锰片表面无明显变化;将锰片插入到氯化铜溶液中,一段时间后观察到锰片表面有红色物质生成.
①根据以上实验判断,三种金属的活动性由强到弱的顺序是Mg>Mn>Cu.
②写出单质锰(Mn)与氧化铜溶液反应的化学方程式Mn+CuCl2═MnCl2+Cu(该化合物中Mn元素显+2价).
(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液,向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有Ag(填化学式),滤液中一定含有的溶质是Fe(NO3)2(填化学式).
(5)在高温下,利用焦炭与氧气反应生成的一氧化碳可把铁从铁矿石里还原出来.某炼铁厂现用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是583.3t.(计算结果精确到0.1)
分析 (1)依据铁生锈的条件分析;
(2)金属材料包括纯金属以及它们的合金,据此结合题意进行分析判断即可.
(3)①根据“活动性较强的金属一般可以将位于其后的金属从它们的盐溶液中置换出来”分析解答.
②根据“活动性较强的金属一般可以将位于其后的金属从它们的盐溶液中置换出来”分析解答;
(4)根据金属活动性顺序可知,三种金属的活动性顺序为:铁、铜、银,所以向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,则铁能与硝酸银反应生成硝酸亚铁和银,能与硝酸铜反应生成硝酸亚铁和铜,向滤渣中滴加稀硫酸,无气泡产生,说明滤渣中一定不含有铁,一定含有银,可能含有铜;滤液中一定含有的溶质是硝酸亚铁进行分析.
(5)由赤铁矿石的质量、氧化铁的质量分数、生铁中杂质的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答 解:
(1)铁生锈的条件:铁与水和氧气同时接触,会导致铁制品的锈蚀.
(2)A、不锈钢是钢的一种,是铁的合金,主要成分是铁,含有碳等其它物质,属于混合物,故选项错误.
B、不锈钢是钢的一种,是铁的合金,属于金属材料,故选项正确.
C、不锈钢是钢的一种,是铁的合金,属于金属材料,不是合成材料,故选项错误.
D、不锈钢是钢的一种,是铁的合金,属于金属材料,不是复合材料,故选项错误.
故选B.
(3)①活动性较强的金属一般可以将位于其后的金属从它们的盐溶液中置换出来.将锰片插入到氯化镁溶液中,一段时间后观察到锰片表面无明显变化,说明锰不能置换出镁,镁的活动性要比锰强;将锰片插入到氯化铜溶液中,一段时间后观察到锰片表面有红色物质生成,说明有可以置换出氯化铜溶液中的铜,锰的活动性比铜强.
所以三种金属的活动性由强到弱的顺序是:Mg>Mn>Cu.
故答案为:Mg>Mn>Cu.
②因为活动性较强的金属一般可以将位于其后的金属从它们的盐溶液中置换出来,所以单质锰(Mn)与氯化铜溶液反应,可以把铜置换出来.
故答案为:Mn+CuCl2═MnCl2+Cu.
(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,则铁能与硝酸银反应生成硝酸亚铁和银,能与硝酸铜反应生成硝酸亚铁和铜,向滤渣中滴加稀硫酸,无气泡产生,说明滤渣中一定不含有铁,一定含有银,可能含有铜;滤液中一定含有的溶质是硝酸亚铁.
(5)由于一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,根据化学方程式进行计算代入的数据必须是纯净物的质量,可设理论上可以炼出的含铁96%的生铁的质量是x,则
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
1000t×80% x×96%
$\frac{160}{1000t×80%}=\frac{112}{x×96%}$
x=583.3t
答案:
(1)氧气;
(2)B;
(3)①Mg>Mn>Cu.
②Mn+CuCl2═MnCl2+Cu.
(4)Ag,Fe(NO3)2.
(5)583.3
点评 本题考查铁生锈的条件、材料的组成、金属的活动性顺序,属于对基础知识的运用.依据金属活动性顺序中位于氢之前的金属能从酸中置换出氢,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来分析即可.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案| A. | 浓溶液 | B. | 稀溶液 | ||
| C. | 不能再继续溶解该溶质的溶液 | D. | 还能继续溶解该物质的溶液 |
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | 铜粉 | 铁粉 | 氧气 | 灼烧 |
| B | 二氧化碳 | 一氧化碳 | 碳粉 | 通过足量灼热碳粉 |
| C | 氯化钾粉末 | 碳酸钾粉末 | 稀盐酸 | 加足量稀盐酸蒸发结晶 |
| D | 盐酸 | 硫酸 | 氢氧化钡溶液 | 加入过量氢氧化钡溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
| 实验编号 | 实验① | 实验② | 实验③ | 实验④ |
| 实验图示 |  |  | 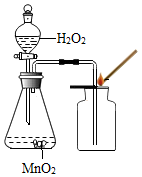 |  |
| 实验编号 | 实验⑤ | 实验⑥ | 实验⑦ | 实验⑧ |
| 实验图示 |  |  |  |  |
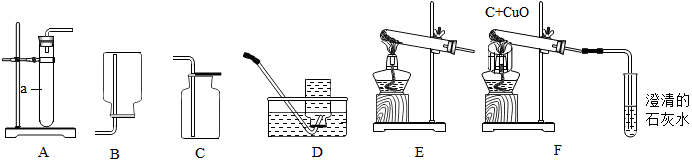
(2)实验②中,预先在集气瓶里装有少量的水,其目的是防止生成物熔化溅落下来炸裂集气瓶.
(3)实验③中,制取气体的化学反应方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;收集气体用向上排空气法,说明制取气体的密度比空气的密度大(填“大”或“小”或“相同”);证明集气瓶里已收集满气体的实验操作方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)实验④中,将溶液进行过滤得操作时,玻璃棒在实验过程中所起的作用是引流.
(5)实验⑤中,观察到烧杯A中溶液逐渐变成红色,该实验的结论是分子在不断运动.
(6)实验⑥中,根据水中白磷没有燃烧的原理,举出生活中一灭火的事例如用灯帽盖灭酒精灯.
(7)实验⑦中,向烧杯里燃着阶梯蜡烛倾倒CO2气体,观察到的现象是下面的蜡烛先熄灭,然后上面的蜡烛才熄灭.
(8)实验⑧中,用于除去CO中少量的CO2,溶液里发生的化学反应方程式是CO2+2NaOH=Na2CO3+H2O.
(1)我国已推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇,作为汽车的燃料.下列叙述正确的是BC(填字母).
A.乙醇汽油是一种新型的化合物 B.乙醇可通过粮食发酵的方法制得
C.使用乙醇汽油能减少有害气体的排放 D.乙醇和汽油都是可再生能源
请写出乙醇燃烧的化学方程式C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(2)公共汽车和出租车的耗油量(均以汽油为燃料)和载客量如表:
| 公共汽车 | 出租车 | |
| 百公里耗油/kg | 17.1 | 9.12 |
| 平均载客量/人 | 30 | 2 |
 水和溶液在生产生活中起着重要的作用
水和溶液在生产生活中起着重要的作用