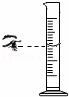题目内容
为检查某石灰石样品中碳酸钙的纯度,取该样品12g放入烧杯中,再向烧杯中加入35g稀盐酸,恰好完全反应(杂质不参加反应),反应后烧杯中剩余固体物质和溶液共42.6g,
(1)反应生成CO2的质量为 g;
(2)石灰石样品中碳酸钙的质量分数.
| 根据化学反应方程式的计算.. | |
| 专题: | 压轴实验题;溶质质量分数与化学方程式相结合的计算. |
| 分析: | 分析所发生的反应,可发现反应后总质量减轻是由于生成了气体二氧化碳,因此,可知恰好完全反应时放出二氧化碳的质量为4.4g;然后利用二氧化碳的质量,根据反应的化学方程式,计算恰好完全反应时碳酸钙的质量,最后使用质量分数的计算公式,求出样品中碳酸钙的质量分数即可. |
| 解答: | 解:(1)恰好完全反应时放出二氧化碳的质量为12g+35g﹣42.6g═4.4g;故填:4.4; (2)设生成4.4gCO2需要碳酸钙的质量为x CaCO3+2HCl═CaCl2+H2O+CO2↑ 100 44 x 4.4g
x=10g
答:石灰石样品中碳酸钙的质量分数为83.33%. |
| 点评: | 根据化学方程式进行计算时,只能使用纯净物的质量进行计算,而不能把混合物的质量直接代入化学方程式进行计算. |

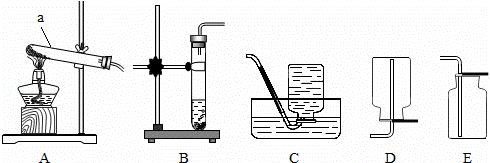
下列实验操作中,错误的是( )
|
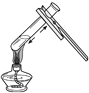
| A. |
给液体加热 | B. |
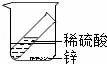
验证质量守恒定律 |
|
| C. |
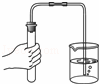
读取液体体积 | D. |
检查装置的气密性 |
除去下列各物质中少量杂质的方法,不合理的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的办法 |
| A | CO2 | CO | 通过足量的灼热氧化铜 |
| B | N2 | O2 | 通过足量的灼热铜网 |
| C | H2 | 水蒸气 | 通过盛有足量浓硫酸的洗气瓶 |
| D | CO2 | HCl | 通过盛有足量氢氧化钠溶液的洗气瓶 |
|
| A. | A | B. | B | C. | C | D. | D |

 ×100%═83.33%
×100%═83.33%