题目内容
请结合下图回答实验室制备气体的问题: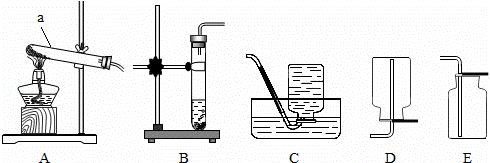
(1)指出仪器名称:a ;
(2)实验室制取氧气可选用的收集装置为 (填字母序号),若选用 装置制备氧气,对应的化学方程式为 ;
(3)用E装置收集二氧化碳,怎样证明二氧化碳已经收集满了 .
| 常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;二氧化碳的检验和验满;书写化学方程式、文字表达式、电离方程式.. | |
| 专题: | 常见气体的实验室制法、检验、干燥与净化. |
| 分析: | (1)要熟悉各种仪器的名称、用途和使用方法; (2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气; 氧气的密度比空气的密度大,不易溶于水; (3)二氧化碳能够溶于水,密度比空气大,不能燃烧,不支持燃烧. |
| 解答: | 解:(1)a是试管,常用作反应容器. 故填:试管. (2)因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用C装置收集; 若选用B装置制备氧气时不需要加热,应该用过氧化氢分解制取氧气,反应的化学方程式为:2H2O2 故填:C或E;B;2H2O2 (3)用E装置收集二氧化碳时,证明二氧化碳已经收集满的方法是:把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满. 故填:把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满. |
| 点评: | 本题综合考查了学生的基本实验能力,涉及仪器的用途、化学方程式的书写、装置选择、实验基本操作等知识,只有综合理解化学知识才能够正确的解答. |

 名校课堂系列答案
名校课堂系列答案某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止。为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳。
[实验一] 选择合适浓度的硫酸
操作:在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为 %,因为浓度小于或大于此浓度对反应的影响是 。
[实验二] 选择合适的反应温度
操作:往盛有1g直径为2mm大理石的大试管中分别加入_________________________________________________________。观察反应的情况,得出结论。
②在合适的硫酸浓度下,应选择最合适的反应温度为70℃。
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加 操作,更有利于气体的制备。
④该研究小组为了研究_______________________对该反应速率的影响,进行了如下实验。
| 试管编号 | A | B |
| 试管内药品 | 1g块状大理石与5mL25%稀硫酸 | 1g粉末状大理石与5mL25%稀硫酸 |
| 现象和比较 | 有少量气泡 | 迅速产生较多气泡 |
Sb2O5是一种重要的阻燃剂.用X来生成该阻燃剂的化学方程式为:X+2H2O2═Sb2O5+2H2O.根据质量守恒定律,推断X的化学式为( )
|
| A. | SbO2 | B. | Sb2O3 | C. | HSbO3 | D. | H3SbO4 |
在天平的左右两个托盘上,各放一质量相等的烧杯,其中盛有等质量、等质量分数的稀硫酸,天平平衡,如果分别将下列四组中的两种物质放入左右两个烧杯内,充分反应后,天平仍保持平衡的是( )
|
| A. | 等质量的锌和铜 |
|
| B. | 等质量的锌和铁(反应后烧杯内酸都有剩余) |
|
| C. | 等质量的锌和铁(反应后烧杯中两种金属均有剩余) |
|
| D. | 等质量的氧化铜和铁 |
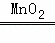 2H2O+O2↑.
2H2O+O2↑. )
) B.CO探测器用于空气质量监测,可以让人们及时了解空气质量状况
B.CO探测器用于空气质量监测,可以让人们及时了解空气质量状况