题目内容
向20g硫酸铜的溶液中投入少量的铁粉,充分反应后过滤得滤液19.6g,则投入铁粉的质量为多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据铁和硫酸铜反应生成硫酸亚铁和铜,然后依据化学反应中溶液质量的变化结合题中所给的数据进行解答.
解答:解:设投入铁粉的质量为x,
Fe+CuSO4=Cu+FeSO4 溶液质量减轻
56 160 152 8
x 20g-19.6g
=
x=2.8g
答:投入铁粉的质量为2.8克.
Fe+CuSO4=Cu+FeSO4 溶液质量减轻
56 160 152 8
x 20g-19.6g
| 56 |
| x |
| 8 |
| 20g-19.6g |
x=2.8g
答:投入铁粉的质量为2.8克.
点评:在解此类题时,首先分析题中的反应原理,然后结合题中所给的数据进行解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
依据如图所示,下列关于电解水实验的叙述正确的是( )
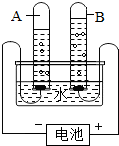

| A、氧气与氢气的体积比是2:1 |
| B、A试管中气体使带火星木条复燃 |
| C、水中氢、氧两种元素的质量比是8:1 |
| D、水是由氢、氧两种元素组成的 |