题目内容
(5分)在20℃时,向质量均为50g的5份水中分别加入一定质量的氯化钾固体,然后搅拌至完全溶解得到溶液。加入氯化钾的质量与所得溶液的质量如下表:
实验编号 | ① | ② | ③ | ④ | ⑤ |
加入氯化钾的质量/g | 5 | 10 | 15 | 20 | 25 |
溶液的质量/g | 55 | 60 | 65 | 67 | 67 |
(1)③中所得溶液是氯化钾的 溶液;(填“饱和”或“不饱和”)
(2)20℃时,50g水中最多能溶解 g氯化钾;
(3)请认真分析上表数据,计算20℃时氯化钾饱和溶液中溶质的质量分数。(要求写出完整的计算过程,结果精确到小数点后一位)
(1)不饱和;(2)17;(3)25.4%.
【解析】(1)根据④、⑤的数据可知,50g水在该温度下最多溶解67g-50g=17g溶质,③所得溶液还能溶解溶质,所以为氯化钾的不饱和溶液;
(2)根据图示的实验数据可知,20℃时,50g水中最多能溶解67g-50g=17g溶质氯化钾;
(3)因为饱和溶液中溶解溶质达到最大量,溶质质量分数也达到最大值,根据题目中的数据可知,20℃时,50g水中最多能溶解67g-50g=17g溶质氯化钾达到饱和状态,所以该饱和溶液的溶质质量分数为: =25.4%
=25.4%
答:20℃时氯化钾饱和溶液中溶质的质量分数为25.4%.
试题分析:根据表格中的数据可知,20℃时50g水中最多溶解67g-50g=17g氯化钾,而③中溶解了15g溶质分析;根据20℃时,50g水中最多能溶解67g-50g=17g溶质氯化钾,根据溶解度的概念及饱和溶液中溶质、溶剂的质量关系计算该温度下氯化钾的溶解度.
考点:饱和溶液与不饱和溶液的判断;溶解度表示的意义;饱和溶液中溶质质量分数的计算方法

(8分)实验室中有甲、乙两瓶过氧化氢溶液,均标有“10%”字样。相同条件下,用这两瓶过氧化氢溶液制取150mL氧气,所用时间明显不同。对此,同学们进行如下探究。
【猜想】两瓶过氧化氢溶液中溶质的质量分数不同
【进行实验】
序号 | 实验装置 | 主要实验步骤 | 实验现象 |
实 验 1 |
| 向两支试管中分别加入等量的甲、乙两瓶中的过氧化氢溶液,对比观察 | 两支试管中均有细微的气泡产生 |
实 验 2 |
| 将两个相同的蜡烛分别点燃后放入两个烧杯中,然后分别向两个烧杯中加入等量的甲、乙两瓶中的过氧化氢溶液,再向过氧化氢溶液中加入等量的二氧化锰固体 | 两烧杯内液体中均产生气泡、有白雾,两烧杯内蜡烛均继续燃烧,但加入甲瓶溶液的烧杯中,蜡烛燃烧得更明亮 |
实 验 3 |
| 向装有等量二氧化锰的两个锥形瓶中分别加入等量的甲、乙两瓶中的过氧化氢溶液 | 两锥形瓶内液体中均产生气泡、有白雾,同时有现象①出现 |
【实验结论】
甲瓶溶液中溶质的质量分数大于乙瓶溶液中溶质的质量分数。
【分析与解释】
(1)实验2和实验3中,均发生反应的化学方程式为 。
(2)实验2中,影响蜡烛燃烧明亮程度的因素是 。
(3)实验3中,现象①为 。
【反思与评价】
(1)实验1未观察到现象明显不同的主要原因是________。
(2)实验2和实验3分别应用了化学科学研究中两种重要的方法,它们是_____和_____。
(3)通过以上实验得到如下启示:影响反应速率的因素有 ;欲使燃着的物质燃烧更旺,可采用的方法是 。
(5分)在“质量守恒定律”的课堂教学中,甲、乙两组同学进行了“化学反应中,反应物与生成物的质量关系”的实验探究。实验装置和选用药品如图所示:
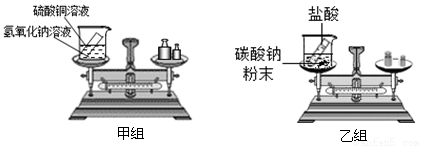
(提示:CuSO4+2NaOH==Na2SO4+Cu(OH)2↓;2HCl+Na2CO3==2NaCl+H2O+CO2↑)
(1)根据实验目的,两组同学应该测量的数据是_____________(填“只有反应前”“只有反应后”“反应前、后”之一)整个反应装罝(包括烧杯、试管和药品)的质量。
(2)实验过程中他们都进行了规范的操作、准确的称量和细致的观察:
现象 | 结论 | |
甲组 | 出现蓝色沉淀,天平平衡 | 质量守恒 |
乙组 | 出现大量气泡,天平不平衡 | 质量不守恒 |
乙组实验反应后天平不平衡,天平指针向 偏转(填“左”或“右”)。你认为结论正确的是 (填“甲组”或“乙组”),而导致另一组结论错误的原因是 。
(3)由质量守恒定律可知,化学反应前后,一定不变的是 。(填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】 H2O2生成O2的快慢与催化剂种类有关
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间。
【进行实验】右下图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是: __________________。
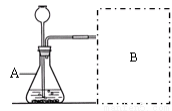
【实验记录】
实验编号 | 1 | 2 |
反应物 | 6% H2O2 | 6% H2O2 |
催化剂 | 1g 红砖粉 | 1g MnO2 |
时间 | 152 s | 35 s |
【结论】该探究过程得出的结论是_______________________________________________。
【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____________和_____________是否改变。